Los estados de la tabla periódica: sólidos, líquidos y gases
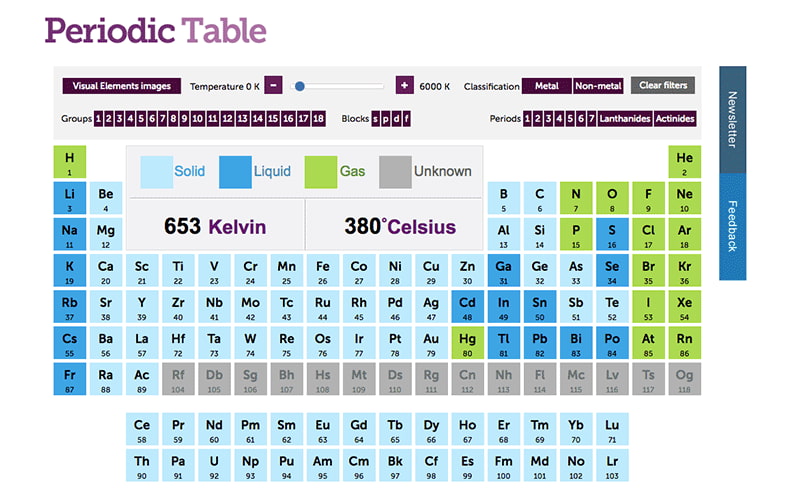
La tabla periódica es una herramienta esencial para entender la química y la física de los elementos que existen en la naturaleza. Y uno de los aspectos más interesantes de la tabla periódica son los estados de la materia que pueden presentar los elementos: sólidos, líquidos y gases.
Cada elemento de la tabla periódica tiene un punto de fusión y un punto de ebullición específicos, lo que determina en qué estado se encuentra a temperatura y presión ambiente. Estos estados de la materia tienen propiedades distintas que los hacen útiles para diferentes aplicaciones.
Sólidos
Los sólidos son aquellos elementos que tienen una estructura cristalina y una forma fija. Es decir, los átomos o iones están organizados en un patrón tridimensional que se repite de manera regular. Los sólidos tienen una densidad alta y no se comprimen fácilmente.
Un ejemplo de elemento sólido es el hierro, que se encuentra en la tabla periódica con el símbolo Fe. El hierro es un metal que se utiliza en la construcción de edificios, en la fabricación de maquinarias y herramientas, y en la producción de acero.
Líquidos
Los líquidos son aquellos elementos que tienen una forma variable y una estructura menos organizada que los sólidos. Los átomos o moléculas de los líquidos se mueven libremente y pueden deslizarse unos sobre otros. Los líquidos tienen una densidad menor que los sólidos y pueden fluir.
Un ejemplo de elemento líquido es el mercurio, que se encuentra en la tabla periódica con el símbolo Hg. El mercurio es un metal líquido que se utiliza en termómetros, interruptores y lámparas fluorescentes.
Gases
Los gases son aquellos elementos que no tienen una forma fija y que se expanden para llenar el espacio disponible. Los átomos o moléculas de los gases se mueven con gran velocidad y tienen una estructura completamente desorganizada. Los gases tienen una densidad muy baja y se pueden comprimir fácilmente.
Un ejemplo de elemento gaseoso es el oxígeno, que se encuentra en la tabla periódica con el símbolo O. El oxígeno es un gas que se utiliza en la respiración de los seres vivos y en la combustión de los combustibles.
Conclusión
Los estados de la materia de la tabla periódica son una parte fundamental de la química y la física. Los sólidos, líquidos y gases tienen propiedades distintas que los hacen útiles para diferentes aplicaciones. Los sólidos son densos y tienen una forma fija, los líquidos fluyen y tienen una forma variable, y los gases se expanden para llenar el espacio disponible y tienen una densidad muy baja. Cada elemento de la tabla periódica tiene un punto de fusión y un punto de ebullición específicos que determinan en qué estado se encuentra a temperatura y presión ambiente.
Preguntas frecuentes
¿Puede un elemento cambiar de estado?
Sí, un elemento puede cambiar de estado al variar su temperatura o presión. Por ejemplo, el agua puede pasar de sólido a líquido a gas a medida que aumenta la temperatura y la presión disminuye.
¿Todos los elementos tienen los tres estados de la materia?
No, algunos elementos sólo tienen un estado de la materia a temperatura y presión ambiente. Por ejemplo, el helio es un gas a temperatura y presión ambiente y no se puede convertir en sólido o líquido sin condiciones extremas.
¿Qué es la sublimación?
La sublimación es el proceso en el que un sólido se convierte directamente en gas sin pasar por el estado líquido. Un ejemplo de sublimación es el hielo seco, que es dióxido de carbono sólido que se sublima a temperatura ambiente.
¿Qué es la condensación?
La condensación es el proceso en el que un gas se convierte en líquido al perder energía térmica. Un ejemplo de condensación es el agua que se forma en el exterior de una botella fría en un día cálido y húmedo.
¿Por qué los gases tienen una densidad tan baja?
Los gases tienen una densidad muy baja porque sus átomos o moléculas se mueven con gran velocidad y tienen una estructura completamente desorganizada. Esto hace que ocupen un espacio mucho mayor que los sólidos o líquidos.
Deja una respuesta