Ley de conservación de la masa: ¡Descubre su importancia!
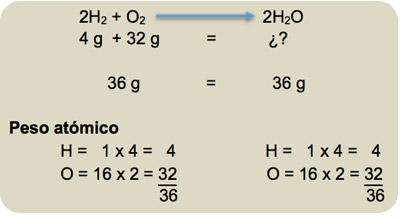
La ley de conservación de la masa es uno de los principios fundamentales de la química. Esta ley establece que la masa de un sistema cerrado no cambia durante una reacción química. En otras palabras, la cantidad de materia que entra en una reacción química es igual a la cantidad de materia que sale de ella.
Pero, ¿por qué es importante la ley de conservación de la masa? En este artículo vamos a profundizar en esta ley y descubrir su importancia en diferentes ámbitos.
- ¿Qué es la ley de conservación de la masa?
- Importancia de la ley de conservación de la masa
- Preguntas frecuentes
- 1. ¿Por qué es importante la ley de conservación de la masa?
- 2. ¿Cómo se aplica la ley de conservación de la masa en la industria química?
- 3. ¿Cómo se relaciona la ley de conservación de la masa con la ley de las proporciones definidas?
- 4. ¿Por qué es importante la ley de conservación de la masa en la seguridad en la industria química?
- 5. ¿Qué es la termodinámica química y cómo se relaciona con la ley de conservación de la masa?
¿Qué es la ley de conservación de la masa?
La ley de conservación de la masa fue descubierta por Antoine Lavoisier en el siglo XVIII. Este principio establece que durante una reacción química, la masa total de los reactantes es igual a la masa total de los productos. Es decir, la masa se conserva.
Esta ley se basa en la idea de que la materia no se crea ni se destruye, sino que se transforma. Durante una reacción química, los átomos de los reactantes se reorganizan para formar nuevos compuestos. Sin embargo, la cantidad total de átomos no cambia, por lo que la masa total del sistema se mantiene constante.
Importancia de la ley de conservación de la masa
La ley de conservación de la masa es fundamental en la química y tiene implicaciones importantes en diferentes ámbitos. A continuación, vamos a explorar algunas de las razones por las que esta ley es tan importante.
1. Permite hacer cálculos precisos
La ley de conservación de la masa permite hacer cálculos precisos sobre las cantidades de reactantes y productos que se necesitan para llevar a cabo una reacción química. Al conocer la masa de los reactantes, se puede predecir la masa de los productos que se van a obtener. Esto es especialmente importante en la industria química, donde se deben producir grandes cantidades de productos de manera eficiente.
2. Ayuda a entender las reacciones químicas
La ley de conservación de la masa también ayuda a entender cómo ocurren las reacciones químicas. Al conocer la cantidad de átomos que se encuentran en los reactantes y productos, se puede entender cómo se reorganizan estos átomos para formar nuevos compuestos.
3. Es esencial para la formulación de leyes químicas
La ley de conservación de la masa es esencial para la formulación de leyes químicas. Por ejemplo, la ley de las proporciones definidas establece que los compuestos siempre contienen los mismos elementos en las mismas proporciones. Esta ley se basa en la idea de que la masa se conserva durante una reacción química.
4. Es importante para la seguridad en la industria química
La ley de conservación de la masa es importante para la seguridad en la industria química. Al conocer la cantidad de reactantes y productos que se van a obtener en una reacción química, se pueden tomar medidas de seguridad adecuadas para evitar accidentes.
5. Es esencial para la comprensión de la termodinámica química
La ley de conservación de la masa es esencial para la comprensión de la termodinámica química. Esta rama de la química se encarga de estudiar los cambios de energía que se producen durante las reacciones químicas. La ley de conservación de la masa es un principio fundamental en la termodinámica, ya que establece que la energía no se crea ni se destruye, sino que se transforma.
Preguntas frecuentes
1. ¿Por qué es importante la ley de conservación de la masa?
La ley de conservación de la masa es importante porque permite hacer cálculos precisos, entender las reacciones químicas, formular leyes químicas, garantizar la seguridad en la industria química y comprender la termodinámica química.
2. ¿Cómo se aplica la ley de conservación de la masa en la industria química?
En la industria química, la ley de conservación de la masa se aplica para calcular las cantidades de reactantes y productos que se necesitan para llevar a cabo una reacción química. Esto permite producir grandes cantidades de productos de manera eficiente y garantizar la seguridad en los procesos químicos.
3. ¿Cómo se relaciona la ley de conservación de la masa con la ley de las proporciones definidas?
La ley de las proporciones definidas establece que los compuestos siempre contienen los mismos elementos en las mismas proporciones. Esta ley se basa en la idea de que la masa se conserva durante una reacción química. Por lo tanto, la ley de conservación de la masa es esencial para la formulación de la ley de las proporciones definidas.
4. ¿Por qué es importante la ley de conservación de la masa en la seguridad en la industria química?
La ley de conservación de la masa es importante en la seguridad en la industria química porque permite conocer las cantidades de reactantes y productos que se van a obtener en una reacción química. Esto permite tomar medidas de seguridad adecuadas para evitar accidentes.
5. ¿Qué es la termodinámica química y cómo se relaciona con la ley de conservación de la masa?
La termodinámica química es la rama de la química que se encarga de estudiar los cambios de energía que se producen durante las reacciones químicas. La ley de conservación de la masa es un principio fundamental en la termodinámica, ya que establece que la energía no se crea ni se destruye, sino que se transforma. Por lo tanto, la ley de conservación de la masa es esencial para la comprensión de la termodinámica química.
Deja una respuesta