La estructura de Lewis del agua: ¡descubre su disposición atómica!
El agua es esencial para la vida tal y como la conocemos. Es una de las sustancias más abundantes en la Tierra y es una molécula única en muchos aspectos. Una de las formas de entender cómo se comporta el agua es a través de su estructura de Lewis. En este artículo, descubriremos la disposición atómica del agua y cómo se representa en su estructura de Lewis.
¿Qué es la estructura de Lewis?
La estructura de Lewis es una representación gráfica de los átomos y electrones en una molécula. Fue desarrollada por el químico estadounidense Gilbert N. Lewis en 1916 y es una herramienta importante en la química orgánica e inorgánica. La estructura de Lewis muestra los átomos de una molécula y los electrones que los rodean.
La estructura de Lewis del agua
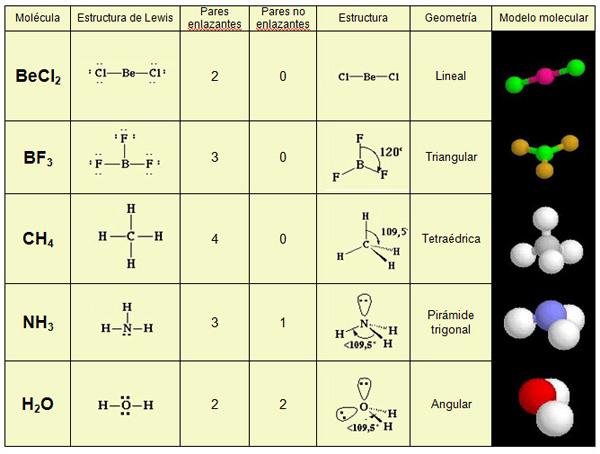
El agua es una molécula compuesta por dos átomos de hidrógeno y uno de oxígeno. La estructura de Lewis del agua muestra los dos átomos de hidrógeno unidos al átomo central de oxígeno mediante enlaces covalentes. Los electrones se representan mediante puntos o líneas y se ubican alrededor de cada átomo.
En la estructura de Lewis del agua, el átomo de oxígeno está rodeado por cuatro electrones solitarios y dos electrones compartidos con cada átomo de hidrógeno. Los electrones compartidos se representan mediante una línea entre los átomos de oxígeno e hidrógeno.
¿Cómo se dibuja la estructura de Lewis del agua?
Para dibujar la estructura de Lewis del agua, se sigue un proceso sencillo. En primer lugar, se escribe la fórmula química del agua, H2O. Luego, se coloca el átomo de oxígeno en el centro y se dibujan los dos átomos de hidrógeno a su alrededor. A continuación, se colocan los electrones alrededor de cada átomo: cuatro electrones solitarios alrededor del oxígeno y un electrón compartido entre el oxígeno y cada átomo de hidrógeno.
¿Qué importancia tiene la estructura de Lewis del agua?
La estructura de Lewis del agua es importante porque nos ayuda a entender cómo se comporta esta molécula en diferentes situaciones. Por ejemplo, podemos ver que el átomo de oxígeno tiene una carga parcial negativa y los átomos de hidrógeno tienen una carga parcial positiva. Esto significa que el agua es una molécula polar y puede interactuar con otras moléculas polares, como los iones.
Además, la estructura de Lewis del agua nos permite entender cómo se forman los enlaces covalentes y cómo se comparten los electrones entre los átomos. Esto es importante en la química y en la comprensión de otras moléculas.
¿Cómo se relaciona la estructura de Lewis del agua con sus propiedades?
La estructura de Lewis del agua está estrechamente relacionada con sus propiedades. Como se mencionó anteriormente, el agua es una molécula polar debido a la disposición de los electrones en su estructura de Lewis. Esto significa que el agua puede disolver otras moléculas polares, como el azúcar o la sal. También es responsable de la tensión superficial del agua, que es la propiedad que permite a algunos insectos caminar sobre la superficie del agua.
La estructura de Lewis también nos permite entender por qué el agua tiene un punto de ebullición alto. Los enlaces covalentes entre los átomos de oxígeno e hidrógeno son fuertes y requieren mucha energía para romperse y convertir el agua líquida en vapor.
Conclusión
La estructura de Lewis del agua es una representación gráfica de los átomos y electrones en esta molécula. Nos permite entender cómo se forman los enlaces covalentes y cómo se comparten los electrones entre los átomos. La estructura de Lewis del agua también está estrechamente relacionada con sus propiedades, como la polaridad, la capacidad de disolver otras moléculas polares y el punto de ebullición alto.
Preguntas frecuentes
1. ¿Por qué se llama estructura de Lewis?
La estructura de Lewis lleva el nombre del químico estadounidense Gilbert N. Lewis, quien la desarrolló en 1916.
2. ¿Qué es un enlace covalente?
Un enlace covalente es un tipo de enlace químico en el que dos átomos comparten un par de electrones.
3. ¿Qué significa que el agua es una molécula polar?
Una molécula polar es aquella en la que los electrones no se comparten de manera uniforme entre los átomos. Esto crea una distribución desigual de cargas eléctricas en la molécula, lo que resulta en una carga parcial positiva en un extremo y una carga parcial negativa en el otro.
4. ¿Cómo se relaciona la estructura de Lewis con otras moléculas?
La estructura de Lewis es una herramienta importante en la química y se utiliza para entender la disposición de átomos y electrones en otras moléculas.
5. ¿Qué otras propiedades tiene el agua que se relacionan con su estructura de Lewis?
La estructura de Lewis del agua también está relacionada con su capacidad para formar puentes de hidrógeno y con su capacidad para actuar como un disolvente universal.
Deja una respuesta