¿Iónico o covalente? Descubre cómo identificarlos
¿Alguna vez te has preguntado cómo se identifican los enlaces iónicos y covalentes? Los enlaces químicos son la base de la formación de moléculas y compuestos, y la diferencia entre un enlace iónico y uno covalente puede cambiar completamente las propiedades de una sustancia. En este artículo, te explicaremos cómo identificar cada tipo de enlace y cómo afecta a las propiedades de los compuestos.
Enlace iónico
Un enlace iónico se forma cuando dos átomos con diferentes electronegatividades se unen. La electronegatividad es la capacidad de un átomo para atraer electrones hacia sí mismo. Si la diferencia de electronegatividad entre dos átomos es mayor de 1,7, se considera que el enlace es iónico.
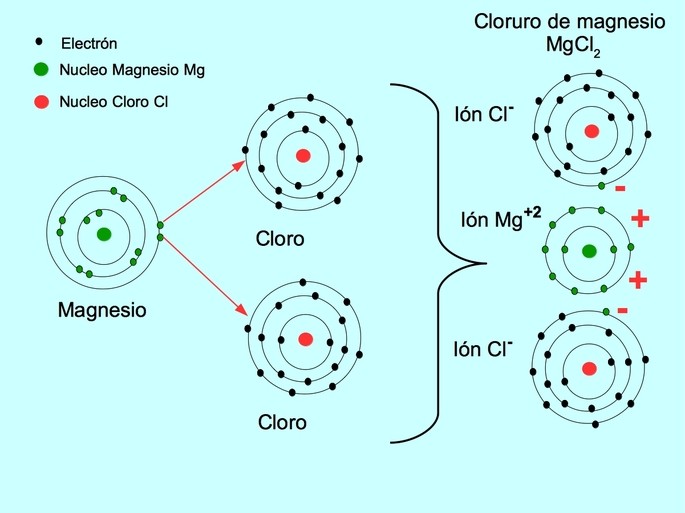
En un enlace iónico, uno de los átomos pierde electrones para convertirse en un catión, y el otro átomo gana electrones para convertirse en un anión. Los iones opuestos se atraen y se mantienen unidos por la fuerza electrostática. Los compuestos iónicos suelen tener altos puntos de fusión y ebullición, son sólidos cristalinos a temperatura ambiente y son solubles en agua.
Un ejemplo de un compuesto iónico es el cloruro de sodio, también conocido como sal de mesa. El sodio (Na) pierde un electrón para convertirse en un catión Na+ y el cloro (Cl) gana un electrón para convertirse en un anión Cl-. La atracción entre los iones Na+ y Cl- forma el compuesto iónico NaCl.
Enlace covalente
En un enlace covalente, dos átomos comparten electrones para formar una molécula. Si los átomos tienen una diferencia de electronegatividad menor de 1,7, se considera que el enlace es covalente.
Los enlaces covalentes pueden ser simples, dobles o triples, dependiendo de la cantidad de electrones compartidos. Los compuestos covalentes suelen tener puntos de fusión y ebullición bajos, son gases o líquidos a temperatura ambiente y no son solubles en agua.
Un ejemplo de un compuesto covalente es el agua (H2O). El hidrógeno (H) y el oxígeno (O) comparten electrones para formar una molécula de agua.
Cómo identificar un enlace iónico o covalente
Para identificar si un enlace es iónico o covalente, se puede utilizar la diferencia de electronegatividad entre los dos átomos. Si la diferencia de electronegatividad es mayor de 1,7, el enlace es iónico. Si la diferencia de electronegatividad es menor de 1,7, el enlace es covalente.
También se puede observar la naturaleza del compuesto. Los compuestos iónicos suelen ser sólidos cristalinos a temperatura ambiente y son solubles en agua. Los compuestos covalentes suelen ser gases o líquidos a temperatura ambiente y no son solubles en agua.
¿Qué pasa cuando hay igualdad de electronegatividad?
En algunos casos, dos átomos tienen igual electronegatividad y forman un enlace covalente no polar. En este tipo de enlace, los electrones se comparten de manera equitativa entre los dos átomos y no hay una carga eléctrica neta. Los compuestos covalentes no polares son solubles en solventes no polares, como la gasolina.
Un ejemplo de un compuesto covalente no polar es el dióxido de carbono (CO2). Los átomos de carbono y oxígeno tienen igual electronegatividad y comparten los electrones de manera equitativa.
Conclusión
La diferencia de electronegatividad entre dos átomos determina si el enlace es iónico o covalente. Los compuestos iónicos suelen ser sólidos cristalinos a temperatura ambiente y son solubles en agua, mientras que los compuestos covalentes suelen ser gases o líquidos a temperatura ambiente y no son solubles en agua. En algunos casos, los átomos tienen igual electronegatividad y forman un enlace covalente no polar.
Preguntas frecuentes
¿Qué es la electronegatividad?
La electronegatividad es la capacidad de un átomo para atraer electrones hacia sí mismo.
¿Qué es un enlace iónico?
Un enlace iónico se forma cuando dos átomos con diferentes electronegatividades se unen. Uno de los átomos pierde electrones para convertirse en un catión, y el otro átomo gana electrones para convertirse en un anión.
¿Qué es un enlace covalente?
En un enlace covalente, dos átomos comparten electrones para formar una molécula.
¿Qué es un compuesto covalente no polar?
En un compuesto covalente no polar, los electrones se comparten de manera equitativa entre dos átomos con igual electronegatividad.
¿Qué propiedades tienen los compuestos iónicos y covalentes?
Los compuestos iónicos suelen ser sólidos cristalinos a temperatura ambiente y son solubles en agua. Los compuestos covalentes suelen ser gases o líquidos a temperatura ambiente y no son solubles en agua.
Deja una respuesta