Electrones en su lugar: Último nivel atómico siempre presente
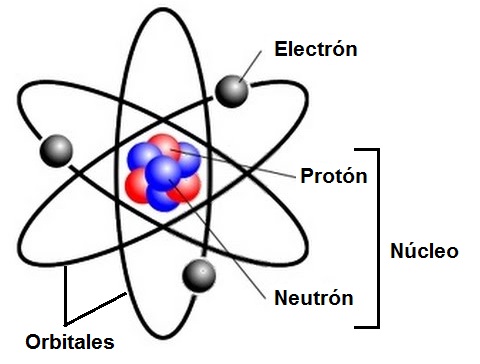
En la teoría atómica, los electrones son las partículas subatómicas que orbitan alrededor del núcleo del átomo. La cantidad de electrones en la capa externa de un átomo determina su comportamiento químico y, por lo tanto, su posición en la tabla periódica de los elementos. Pero, ¿qué sucede con los electrones en el último nivel atómico y por qué son importantes?
En este artículo, exploraremos el papel de los electrones en el último nivel atómico y su importancia en la química y la física.
- ¿Qué es el último nivel atómico?
- ¿Por qué los electrones en el último nivel atómico son importantes?
- ¿Cómo se determina la cantidad de electrones en el último nivel atómico?
- ¿Cómo se comportan los electrones en el último nivel atómico?
- ¿Cómo afecta la presencia de electrones en el último nivel atómico a la conductividad eléctrica?
- Conclusion
- Preguntas frecuentes
¿Qué es el último nivel atómico?
El último nivel atómico, también conocido como capa de valencia, es la capa más externa de un átomo. Esta capa contiene los electrones que están más alejados del núcleo y, por lo tanto, tienen la menor fuerza de atracción hacia él.
Cada átomo tiene diferentes capas de electrones, y la cantidad de electrones en la capa de valencia determina la reactividad química del átomo. Los elementos que tienen la misma cantidad de electrones en su capa de valencia se encuentran en la misma columna de la tabla periódica y tienen propiedades químicas similares.
¿Por qué los electrones en el último nivel atómico son importantes?
Los electrones en el último nivel atómico son importantes porque determinan la reactividad química de un átomo. Estos electrones están más alejados del núcleo y, por lo tanto, son más fácilmente accesibles para interactuar con otros átomos.
Cuando dos átomos se acercan, los electrones de sus capas de valencia pueden interactuar entre sí para formar enlaces químicos. Los enlaces químicos son la base de la química y la vida misma, ya que son responsables de la formación de moléculas y compuestos.
Además, los electrones en el último nivel atómico también están involucrados en la conducción eléctrica y en la transmisión de señales nerviosas en el cuerpo humano.
¿Cómo se determina la cantidad de electrones en el último nivel atómico?
La cantidad de electrones en la capa de valencia se puede determinar mirando la posición del elemento en la tabla periódica. La posición del elemento en la tabla periódica indica la cantidad de capas de electrones que tiene el átomo y la cantidad de electrones en la capa de valencia.
Por ejemplo, el hidrógeno se encuentra en la primera columna de la tabla periódica y tiene un solo electrón en su capa de valencia. El oxígeno, por otro lado, se encuentra en la sexta columna y tiene seis electrones en su capa de valencia.
¿Cómo se comportan los electrones en el último nivel atómico?
Los electrones en la capa de valencia tienen una mayor energía y, por lo tanto, son más reactivos que los electrones en capas internas. Estos electrones pueden interactuar con los electrones de otras capas de valencia para formar enlaces químicos.
Además, los electrones en la capa de valencia pueden ser fácilmente removidos o compartidos con otros átomos, lo que les da la capacidad de conducir electricidad y formar compuestos químicos.
¿Cómo afecta la presencia de electrones en el último nivel atómico a la conductividad eléctrica?
La presencia de electrones en la capa de valencia es esencial para la conductividad eléctrica. Los metales son buenos conductores de electricidad porque tienen electrones libres en su capa de valencia que pueden moverse fácilmente a través del material.
Por otro lado, los materiales aislantes no tienen electrones libres en su capa de valencia y, por lo tanto, no pueden conducir electricidad. Los semiconductores, como el silicio, tienen un número limitado de electrones libres en su capa de valencia y pueden conducir electricidad bajo ciertas condiciones.
Conclusion
Los electrones en el último nivel atómico son esenciales para la química y la física, ya que determinan la reactividad química de un átomo, la conductividad eléctrica y la transmisión de señales nerviosas en el cuerpo humano. La cantidad de electrones en la capa de valencia se puede determinar mirando la posición del elemento en la tabla periódica. Los electrones en la capa de valencia tienen una mayor energía y son más reactivos que los electrones en capas internas.
Preguntas frecuentes
1. ¿Qué sucede si un átomo no tiene electrones en la capa de valencia?
Si un átomo no tiene electrones en su capa de valencia, no puede formar enlaces químicos y es químicamente inerte. Los gases nobles, como el helio y el neón, son ejemplos de elementos con una capa de valencia completa y son químicamente inertes.
2. ¿Por qué los electrones en la capa de valencia tienen una mayor energía?
Los electrones en la capa de valencia tienen una mayor energía porque están más alejados del núcleo y experimentan una fuerza de atracción menor que los electrones en capas internas.
3. ¿Qué son los enlaces químicos?
Los enlaces químicos son la interacción entre los electrones de dos o más átomos que resulta en la formación de una molécula o compuesto.
4. ¿Qué es la conductividad eléctrica?
La conductividad eléctrica es la capacidad de un material para conducir electricidad. Los materiales que tienen electrones libres en su capa de valencia son buenos conductores de electricidad.
5. ¿Por qué los metales son buenos conductores de electricidad?
Los metales son buenos conductores de electricidad porque tienen electrones libres en su capa de valencia que pueden moverse fácilmente a través del material.
Deja una respuesta