Descubre qué produce la reacción ácido-base en química
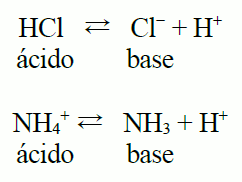
La química es una rama de la ciencia que estudia las propiedades y comportamientos de diferentes elementos y compuestos. Una de las reacciones químicas más comunes es la reacción ácido-base. Esta reacción es esencial para muchos procesos químicos y biológicos, y entender cómo funciona puede ser útil en una variedad de campos.
¿Qué es una reacción ácido-base?
Una reacción ácido-base es una reacción química que involucra un ácido y una base. En una reacción ácido-base, el ácido y la base se neutralizan entre sí y producen agua y una sal. En términos generales, un ácido es una sustancia que puede donar un protón (un ion de hidrógeno), mientras que una base es una sustancia que puede aceptar un protón.
¿Cómo se produce una reacción ácido-base?
Una reacción ácido-base se produce cuando un ácido y una base se combinan. El ácido dona un protón a la base, lo que resulta en la formación de un ion hidrógeno y un ion negativo de la base. El ion hidrógeno se combina con agua y forma un ion hidronio (H3O+). El ion negativo de la base se combina con un ion positivo de la sal para formar la sal y agua.
¿Qué es un ácido?
Un ácido es una sustancia que puede donar un protón (un ion de hidrógeno) a otra sustancia. Los ácidos se caracterizan por su sabor agrio y su capacidad para corroer metales y otros materiales. Los ácidos también pueden cambiar el color de ciertos indicadores, como el papel de tornasol o el fenolftaleína.
¿Qué es una base?
Una base es una sustancia que puede aceptar un protón (un ion de hidrógeno) de otra sustancia. Las bases se caracterizan por su sabor amargo y su capacidad para neutralizar los ácidos. Las bases también pueden cambiar el color de ciertos indicadores, como el papel de tornasol o el fenolftaleína.
¿Cómo se clasifican los ácidos y las bases?
Los ácidos y las bases se pueden clasificar en varios tipos diferentes. Algunos de los tipos más comunes incluyen:
Ácidos fuertes y débiles
Los ácidos fuertes son ácidos que se disocian completamente en solución acuosa, lo que significa que todos los átomos de hidrógeno se separan de la molécula del ácido. Los ácidos débiles se disocian solo parcialmente en solución acuosa, lo que significa que algunos átomos de hidrógeno permanecen unidos a la molécula del ácido.
Bases fuertes y débiles
Las bases fuertes son bases que se disocian completamente en solución acuosa, lo que significa que todos los iones hidróxido (OH-) se separan de la molécula de la base. Las bases débiles se disocian solo parcialmente en solución acuosa, lo que significa que algunos iones hidróxido permanecen unidos a la molécula de la base.
Ácidos y bases monopróticos y polipróticos
Los ácidos y las bases monopróticos son aquellos que pueden donar o aceptar un solo protón. Los ácidos y las bases polipróticos son aquellos que pueden donar o aceptar más de un protón.
¿Por qué son importantes las reacciones ácido-base?
Las reacciones ácido-base son importantes por varias razones. En primer lugar, son esenciales para la vida. La mayoría de los procesos biológicos, como la digestión y la respiración, dependen de las reacciones ácido-base. Las reacciones ácido-base también son importantes para la industria, ya que se utilizan para producir una amplia variedad de productos, desde alimentos y medicamentos hasta productos químicos y plásticos.
Conclusión
La reacción ácido-base es una reacción química que involucra un ácido y una base. Cuando se combinan, el ácido y la base se neutralizan entre sí y producen agua y una sal. Las reacciones ácido-base son esenciales para muchos procesos biológicos y son importantes en la industria.
Preguntas frecuentes
1. ¿Cuáles son algunos ejemplos de ácidos?
Algunos ejemplos comunes de ácidos incluyen el ácido clorhídrico (HCl), el ácido sulfúrico (H2SO4) y el ácido acético (CH3COOH).
2. ¿Cuáles son algunos ejemplos de bases?
Algunos ejemplos comunes de bases incluyen el hidróxido de sodio (NaOH), el hidróxido de calcio (Ca(OH)2) y el hidróxido de amonio (NH4OH).
3. ¿Qué es una solución ácida?
Una solución ácida es una solución que tiene un pH menor que 7. Las soluciones ácidas tienen un exceso de iones hidrógeno (H+) y un déficit de iones hidróxido (OH-).
4. ¿Qué es una solución básica?
Una solución básica es una solución que tiene un pH mayor que 7. Las soluciones básicas tienen un exceso de iones hidróxido (OH-) y un déficit de iones hidrógeno (H+).
5. ¿Qué es el pH?
El pH es una medida de la acidez o la basicidad de una solución. El pH se mide en una escala de 0 a 14, donde 0 es extremadamente ácido, 7 es neutral y 14 es extremadamente básico.
Deja una respuesta