Descubre los grupos y familias en la tabla periódica
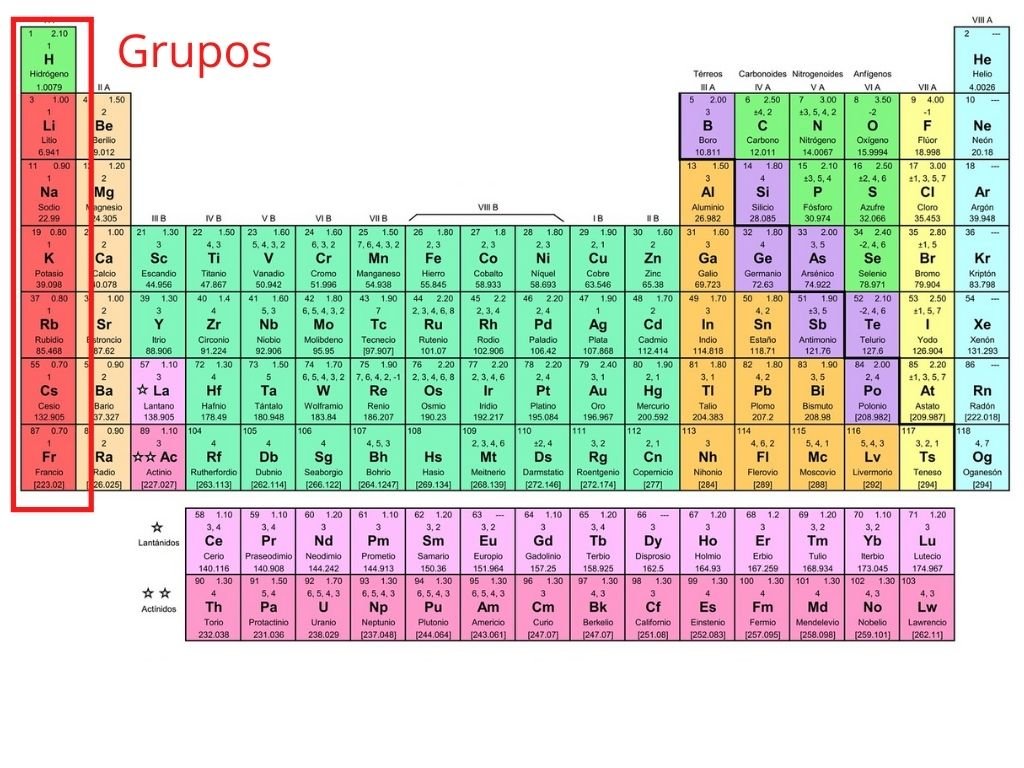
La tabla periódica es una herramienta esencial para los químicos y estudiantes de química. En ella, se encuentran todos los elementos conocidos por el hombre, ordenados por su número atómico, símbolo y masa atómica. Pero, además de esto, la tabla periódica también se divide en grupos y familias, lo que nos ayuda a entender mejor las propiedades de los elementos y su comportamiento en reacciones químicas. En este artículo, vamos a descubrir qué son los grupos y familias en la tabla periódica.
Grupos en la tabla periódica
La tabla periódica se divide en 18 grupos, que se numeran del 1 al 18. Estos grupos se organizan de manera vertical en la tabla, y los elementos que pertenecen a un mismo grupo tienen propiedades químicas y físicas similares. Cada grupo se identifica por un número romano y una letra mayúscula, que se encuentra en la parte superior de la columna.
Grupo 1: Metales alcalinos
El grupo 1 de la tabla periódica se conoce como los metales alcalinos. Estos elementos son altamente reactivos y tienen un solo electrón en su capa externa. Los metales alcalinos son muy blandos y tienen un bajo punto de fusión. Algunos ejemplos de metales alcalinos son el sodio (Na), el potasio (K) y el litio (Li).
Grupo 2: Metales alcalinotérreos
El grupo 2 de la tabla periódica se conoce como los metales alcalinotérreos. Estos elementos también son altamente reactivos, pero un poco menos que los metales alcalinos. Tienen dos electrones en su capa externa y son bastante duros. Algunos ejemplos de metales alcalinotérreos son el calcio (Ca), el magnesio (Mg) y el berilio (Be).
Grupo 3-12: Metales de transición
Los elementos del grupo 3 al 12 se conocen como los metales de transición. Estos elementos son conocidos por su alta densidad, punto de fusión y dureza. También son buenos conductores de electricidad y se utilizan en una amplia variedad de aplicaciones, desde joyería hasta construcción y electrónica. Algunos ejemplos de metales de transición son el hierro (Fe), el cobre (Cu) y el oro (Au).
Grupo 13: Grupo del boro
El grupo 13 de la tabla periódica se conoce como el grupo del boro. Estos elementos tienen tres electrones en su capa externa y son bastante reactivos. El boro (B) es el elemento más conocido de este grupo.
Grupo 14: Grupo del carbono
El grupo 14 de la tabla periódica se conoce como el grupo del carbono. El carbono es el elemento más conocido de este grupo y es esencial para la vida en la Tierra. Otros elementos de este grupo incluyen el silicio (Si), el germanio (Ge) y el estaño (Sn).
Grupo 15: Grupo del nitrógeno
El grupo 15 de la tabla periódica se conoce como el grupo del nitrógeno. Estos elementos tienen cinco electrones en su capa externa y son importantes para la vida en la Tierra. El nitrógeno (N) es el elemento más conocido de este grupo.
Grupo 16: Grupo del oxígeno
El grupo 16 de la tabla periódica se conoce como el grupo del oxígeno. Estos elementos tienen seis electrones en su capa externa y son esenciales para la vida en la Tierra. El oxígeno (O) es el elemento más conocido de este grupo.
Grupo 17: Halógenos
El grupo 17 de la tabla periódica se conoce como los halógenos. Estos elementos son altamente reactivos y tienen siete electrones en su capa externa. Los halógenos son importantes para nuestra salud y bienestar, y se utilizan en una amplia variedad de aplicaciones, desde la medicina hasta la industria. Algunos ejemplos de halógenos son el cloro (Cl), el flúor (F) y el yodo (I).
Grupo 18: Gases nobles
El grupo 18 de la tabla periódica se conoce como los gases nobles. Estos elementos son muy estables y no reactivos. Se utilizan en una amplia variedad de aplicaciones, desde la iluminación hasta la exploración espacial. Algunos ejemplos de gases nobles son el helio (He), el argón (Ar) y el xenón (Xe).
Familias en la tabla periódica
Además de los grupos, la tabla periódica también se divide en familias. Las familias se basan en las similitudes de la configuración electrónica de los elementos. A continuación, se presentan algunas de las familias más importantes en la tabla periódica.
Familia del litio
La familia del litio se encuentra en el grupo 1 de la tabla periódica. Incluye el litio (Li), el sodio (Na), el potasio (K), el rubidio (Rb), el cesio (Cs) y el francio (Fr). Todos los elementos de esta familia tienen un electrón en su capa externa.
Familia del berilio
La familia del berilio se encuentra en el grupo 2 de la tabla periódica. Incluye el berilio (Be), el magnesio (Mg), el calcio (Ca), el estroncio (Sr), el bario (Ba) y el radio (Ra). Todos los elementos de esta familia tienen dos electrones en su capa externa.
Familia del carbono
La familia del carbono se encuentra en el grupo 14 de la tabla periódica. Incluye el carbono (C), el silicio (Si), el germanio (Ge), el estaño (Sn) y el plomo (Pb). Todos los elementos de esta familia tienen cuatro electrones en su capa externa.
Familia del nitrógeno
La familia del nitrógeno se encuentra en el grupo 15 de la tabla periódica. Incluye el nitrógeno (N), el fósforo (P), el arsénico (As), el antimonio (Sb) y el bismuto (Bi). Todos los elementos de esta familia tienen cinco electrones en su capa externa.
Familia del oxígeno
La familia del oxígeno se encuentra en el grupo 16 de la tabla periódica. Incluye el oxígeno (O), el azufre (S), el selenio (Se), el telurio (Te) y el polonio (Po). Todos los elementos de esta familia tienen seis electrones en su capa externa.
Familia de los halógenos
La familia de los halógenos se encuentra en el grupo 17 de la tabla periód
Deja una respuesta