Descubre las partículas subatómicas clave del átomo
El átomo es la unidad básica de la materia, pero ¿sabes qué lo compone? En este artículo, te hablaremos sobre las partículas subatómicas clave del átomo, sus características y su función en la estructura atómica.
Los componentes del átomo
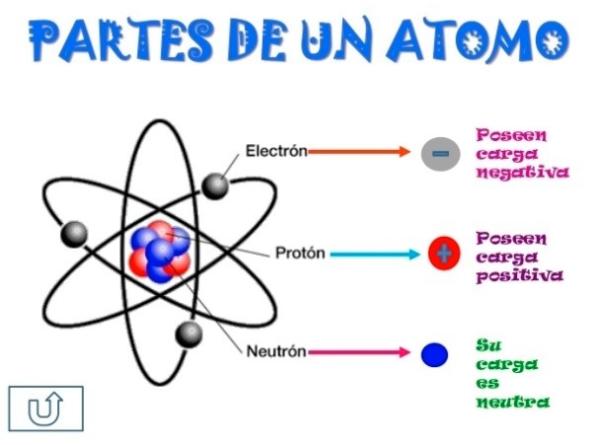
Un átomo está compuesto por tres partículas subatómicas: protones, neutrones y electrones. Los protones y los neutrones se encuentran en el núcleo del átomo, mientras que los electrones orbitan alrededor del núcleo.
Protones
Los protones tienen una carga positiva y una masa de aproximadamente 1 unidad de masa atómica. La cantidad de protones en el núcleo de un átomo determina su número atómico, que a su vez define qué elemento químico es. Por ejemplo, si un átomo tiene 6 protones en su núcleo, pertenece al elemento carbono.
Neutrones
Los neutrones tienen una carga neutra y una masa de aproximadamente 1 unidad de masa atómica. A diferencia de los protones, el número de neutrones en el núcleo puede variar en un mismo elemento químico, lo que se conoce como isótopos. La cantidad de neutrones en un átomo puede afectar su estabilidad y su capacidad para formar enlaces químicos.
Electrones
Los electrones tienen una carga negativa y una masa extremadamente pequeña. Orbitan alrededor del núcleo en diferentes niveles de energía, llamados capas electrónicas. La cantidad de electrones en la capa más externa de un átomo determina su comportamiento químico y su capacidad para formar enlaces con otros átomos.
La estructura atómica
La estructura atómica se refiere a cómo están dispuestas estas partículas subatómicas en un átomo. El núcleo, formado por protones y neutrones, está rodeado por una nube de electrones en movimiento constante.
El modelo de Bohr
El modelo de Bohr fue propuesto en 1913 por el físico danés Niels Bohr. Este modelo describe el átomo como un sistema solar en miniatura, en el que los electrones orbitan alrededor del núcleo en capas definidas por su energía. Cada capa puede contener un número máximo de electrones y, cuando se llena, el siguiente electrón se coloca en la capa siguiente.
El modelo actual
El modelo actual de la estructura atómica es más complejo y se basa en la mecánica cuántica. Según este modelo, los electrones no se mueven en órbitas definidas, sino que se encuentran en una nube de probabilidad alrededor del núcleo. Esta nube de probabilidad se llama orbital y define la posición y la energía del electrón en un momento determinado.
La importancia de las partículas subatómicas
Las partículas subatómicas son esenciales para entender cómo funciona el mundo a nuestro alrededor. El comportamiento de los átomos y las moléculas está directamente relacionado con la cantidad y la disposición de estas partículas.
La química
La química se basa en la interacción de los átomos y las moléculas. La disposición de los electrones en la capa más externa de un átomo determina su capacidad para formar enlaces químicos con otros átomos. La forma en que se unen los átomos y las moléculas influye en las propiedades físicas y químicas de las sustancias.
La física
La física también se beneficia del estudio de las partículas subatómicas. El comportamiento de los electrones y los átomos a nivel subatómico puede explicar fenómenos físicos como la conductividad eléctrica y la fluorescencia.
Preguntas frecuentes
¿Qué son las partículas subatómicas?
Las partículas subatómicas son las partículas más pequeñas que componen la materia. Incluyen protones, neutrones y electrones.
¿Por qué son importantes las partículas subatómicas?
Las partículas subatómicas son importantes porque determinan la estructura y el comportamiento de los átomos y las moléculas, lo que a su vez influye en las propiedades físicas y químicas de los materiales.
¿Cómo se relacionan los protones y los electrones en un átomo?
Los protones tienen una carga positiva y los electrones tienen una carga negativa. Debido a su carga opuesta, los protones y los electrones se atraen entre sí y se mantienen unidos en un átomo.
¿Qué es un isótopo?
Un isótopo es un átomo de un elemento químico que tiene el mismo número de protones en su núcleo, pero difiere en el número de neutrones. Por lo tanto, los isótopos tienen la misma carga nuclear, pero diferentes masas atómicas.
¿Cómo se determina el número atómico de un elemento?
El número atómico de un elemento se determina por la cantidad de protones en su núcleo. Este número define qué elemento químico es. Por ejemplo, si un átomo tiene 6 protones en su núcleo, pertenece al elemento carbono.
Deja una respuesta