Descubre las partes de un elemento en la tabla periódica
La tabla periódica es una herramienta esencial para cualquier estudiante de química o científico. Contiene información valiosa sobre los elementos, sus propiedades y su comportamiento químico. Pero, ¿sabes realmente cómo está organizada la tabla periódica y qué representan sus partes? En este artículo, exploraremos las diferentes secciones de la tabla periódica y lo que significan.
- ¿Qué es la tabla periódica?
- Partes de la tabla periódica
- 1. Símbolo del elemento
- 2. Número atómico
- 3. Masa atómica
- 4. Grupos
- 5. Períodos
- 6. Bloques de elementos
- 7. Elementos de transición
- 8. Elementos representativos
- 9. Elementos de tierras raras
- 10. Gases nobles
- 11. Elementos halógenos
- 12. Metales alcalinos
- 13. Metales alcalinotérreos
- 14. Lantánidos
- 15. Actínidos
- Conclusión
- Preguntas frecuentes
¿Qué es la tabla periódica?
La tabla periódica es una organización de los elementos químicos en una disposición específica. Los elementos se colocan en filas y columnas según sus propiedades químicas y físicas. Está diseñada para mostrar las tendencias y patrones en las propiedades de los elementos.
Partes de la tabla periódica
La tabla periódica consta de varias partes clave que ayudan a los científicos a comprender las propiedades y comportamientos de los elementos. A continuación, se detallan algunas de las partes más importantes de la tabla periódica.
1. Símbolo del elemento
Cada elemento en la tabla periódica tiene un símbolo único que lo identifica. El símbolo a menudo es una abreviatura del nombre del elemento, como el símbolo "O" para oxígeno o "Na" para sodio.
2. Número atómico
El número atómico es la cantidad de protones que tiene un átomo del elemento. En la tabla periódica, los elementos se organizan en orden creciente según su número atómico. El número atómico es importante porque determina las propiedades únicas de cada elemento.
3. Masa atómica
La masa atómica es la masa total de un átomo del elemento, incluyendo protones, neutrones y electrones. La masa atómica se expresa en unidades de masa atómica (uma) y se redondea al número entero más cercano. La masa atómica se utiliza para calcular la masa molar de los elementos.
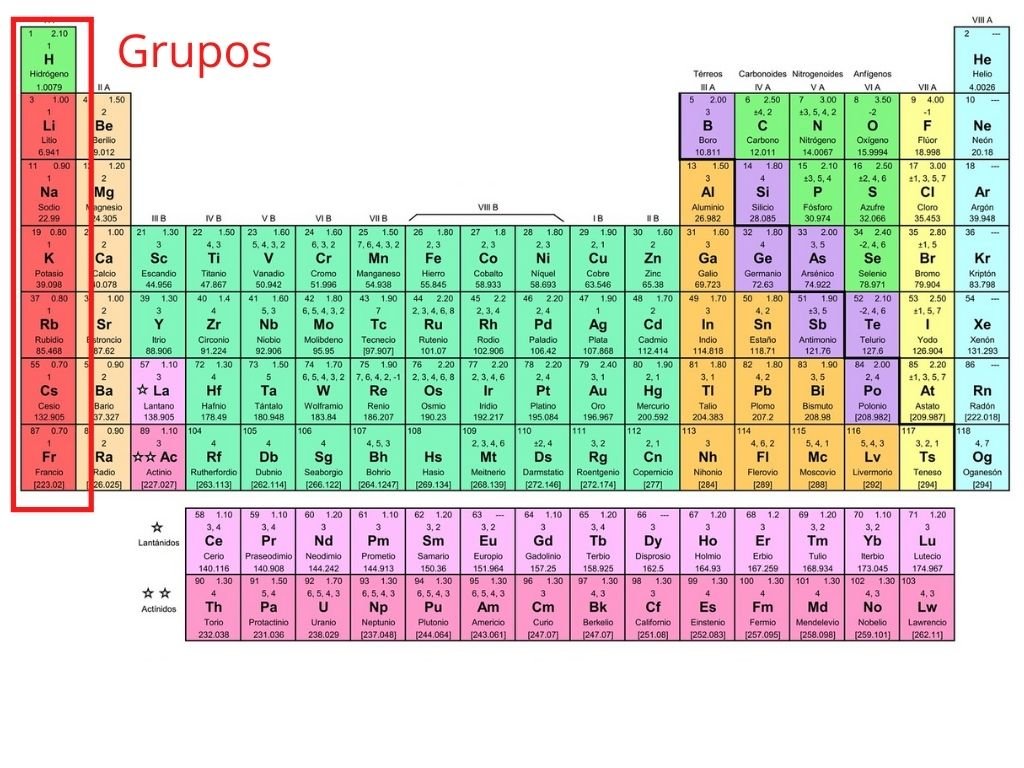
4. Grupos
Los grupos son las columnas verticales de la tabla periódica. Los elementos en un grupo tienen propiedades químicas y físicas similares debido a su configuración electrónica similar. Hay 18 grupos en la tabla periódica.
5. Períodos
Los períodos son las filas horizontales de la tabla periódica. Los elementos en un período tienen propiedades diferentes debido a sus configuraciones electrónicas únicas. Hay siete períodos en la tabla periódica.
6. Bloques de elementos
Los bloques de elementos son secciones de la tabla periódica que contienen elementos con la misma configuración electrónica en sus orbitales externos. Hay cuatro bloques en la tabla periódica: s, p, d y f.
7. Elementos de transición
Los elementos de transición son los elementos en los bloques d y f de la tabla periódica. Tienen propiedades únicas debido a su configuración electrónica y se utilizan en una variedad de aplicaciones industriales y científicas.
8. Elementos representativos
Los elementos representativos son los elementos en los bloques s y p de la tabla periódica. Tienen propiedades químicas y físicas únicas y se utilizan en una variedad de aplicaciones industriales y científicas.
9. Elementos de tierras raras
Los elementos de tierras raras son los elementos en el bloque f de la tabla periódica. Son metales raros y se utilizan en una variedad de aplicaciones industriales y científicas.
10. Gases nobles
Los gases nobles son los elementos en el Grupo 18 de la tabla periódica. Tienen una configuración electrónica estable y no reactiva y se utilizan en una variedad de aplicaciones científicas y tecnológicas.
11. Elementos halógenos
Los elementos halógenos son los elementos en el Grupo 17 de la tabla periódica. Son altamente reactivos y se utilizan en una variedad de aplicaciones industriales y científicas.
12. Metales alcalinos
Los metales alcalinos son los elementos en el Grupo 1 de la tabla periódica. Son altamente reactivos y se utilizan en una variedad de aplicaciones industriales y científicas.
13. Metales alcalinotérreos
Los metales alcalinotérreos son los elementos en el Grupo 2 de la tabla periódica. Son menos reactivos que los metales alcalinos y se utilizan en una variedad de aplicaciones industriales y científicas.
14. Lantánidos
Los lantánidos son los elementos en la serie lantánida de la tabla periódica. Son metales raros y se utilizan en una variedad de aplicaciones industriales y científicas.
15. Actínidos
Los actínidos son los elementos en la serie actínida de la tabla periódica. Son metales raros y se utilizan en una variedad de aplicaciones científicas y tecnológicas.
Conclusión
La tabla periódica es una herramienta esencial para cualquier estudiante de química o científico. Contiene información valiosa sobre los elementos, sus propiedades y su comportamiento químico. Al comprender las diferentes secciones de la tabla periódica, puede obtener una mejor comprensión de la química y utilizarla en sus estudios o investigaciones.
Preguntas frecuentes
1. ¿Por qué es importante conocer las partes de la tabla periódica?
Es importante conocer las partes de la tabla periódica porque permite a los estudiantes de química y científicos comprender mejor las propiedades y comportamientos de los elementos.
2. ¿Cómo están organizados los elementos en la tabla periódica?
Los elementos se organizan en filas y columnas según sus propiedades químicas y físicas.
3. ¿Qué es un número atómico?
El número atómico es la cantidad de protones que tiene un átomo del elemento. Es importante porque determina las propiedades únicas de cada elemento.
4. ¿Qué son los bloques de elementos en la tabla periódica?
Los bloques de elementos son secciones de la tabla periódica que contienen elementos con la misma configuración electrónica en sus orbitales externos.
5. ¿Qué son los metales alcalinos?
Los metales alcalinos son los elementos en el Grupo 1 de la tabla periódica. Son altamente reactivos y se utilizan en una variedad de aplicaciones industriales y científicas.
Deja una respuesta