Descubre la variación del carácter metálico en la tabla periódica
La tabla periódica es una herramienta indispensable para la química y la física, ya que nos permite entender y predecir el comportamiento de los elementos en función de sus propiedades. Una de las características más importantes de los elementos es su carácter metálico, que varía de un extremo a otro de la tabla periódica. En este artículo, te explicaremos qué es el carácter metálico, cómo se mide y cómo varía en la tabla periódica.
¿Qué es el carácter metálico?
El carácter metálico se refiere a la tendencia de un átomo de ceder electrones y formar iones positivos. Los metales tienen un carácter metálico alto, lo que significa que tienen una fuerte tendencia a ceder electrones y formar iones positivos. Por otro lado, los no metales tienen un carácter metálico bajo, lo que significa que tienen una tendencia mucho menor a ceder electrones y formar iones positivos.
¿Cómo se mide el carácter metálico?
El carácter metálico se puede medir de varias maneras. Una forma común es mediante la energía de ionización, que es la energía necesaria para remover un electrón de un átomo neutro. Los metales tienen una energía de ionización baja, lo que significa que es fácil remover un electrón de ellos. Por otro lado, los no metales tienen una energía de ionización alta, lo que significa que es difícil remover un electrón de ellos.
Otra forma de medir el carácter metálico es mediante la electronegatividad, que es la capacidad de un átomo para atraer electrones hacia sí mismo. Los metales tienen una electronegatividad baja, lo que significa que no atraen electrones con mucha fuerza. Los no metales tienen una electronegatividad alta, lo que significa que atraen electrones con mucha fuerza.
¿Cómo varía el carácter metálico en la tabla periódica?
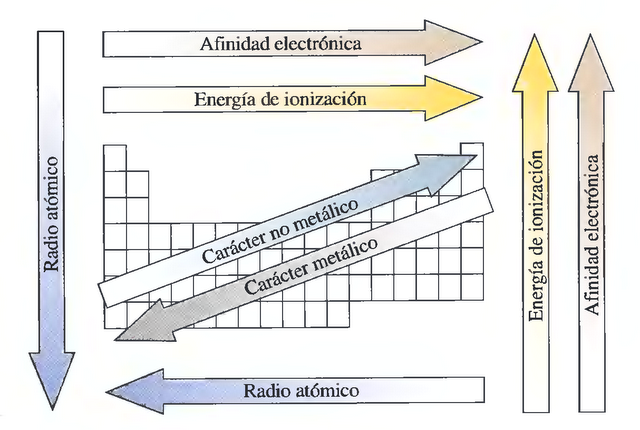
El carácter metálico varía de manera sistemática en la tabla periódica. En general, el carácter metálico aumenta de derecha a izquierda en un período y de abajo hacia arriba en un grupo. Esto se debe a la variación en la carga nuclear efectiva, que es la carga nuclear que siente un electrón en un átomo debido a la presencia de otros electrones en el mismo átomo. Cuanto mayor es la carga nuclear efectiva, mayor es la atracción que siente un electrón hacia el núcleo del átomo, lo que disminuye el carácter metálico.
En los períodos, el carácter metálico disminuye de izquierda a derecha porque la carga nuclear efectiva aumenta. En los grupos, el carácter metálico aumenta hacia abajo porque los electrones se encuentran en capas cada vez más alejadas del núcleo, lo que disminuye la carga nuclear efectiva.
Grupo 1: Los metales alcalinos
En el grupo 1 de la tabla periódica se encuentran los metales alcalinos, que son los elementos más metálicos de la tabla periódica. Estos elementos tienen una electronegatividad baja y una energía de ionización baja, lo que significa que tienen una fuerte tendencia a ceder electrones y formar iones positivos. Los metales alcalinos son muy reactivos y reaccionan vigorosamente con el agua y otros compuestos.
Grupo 2: Los metales alcalinotérreos
En el grupo 2 de la tabla periódica se encuentran los metales alcalinotérreos, que también son muy metálicos pero tienen un carácter metálico ligeramente menor que los metales alcalinos. Estos elementos tienen una electronegatividad baja y una energía de ionización baja, lo que significa que tienen una fuerte tendencia a ceder electrones y formar iones positivos. Los metales alcalinotérreos también son reactivos, pero menos que los metales alcalinos.
Grupo 13: Los metales del grupo del boro
En el grupo 13 de la tabla periódica se encuentran los metales del grupo del boro, que tienen un carácter metálico menor que los metales alcalinotérreos. Estos elementos tienen una electronegatividad ligeramente mayor y una energía de ionización ligeramente mayor que los metales alcalinotérreos, lo que significa que tienen una menor tendencia a ceder electrones y formar iones positivos.
Grupo 14: Los elementos del grupo del carbono
En el grupo 14 de la tabla periódica se encuentran los elementos del grupo del carbono, que son los elementos más importantes para la vida y la química orgánica. Estos elementos tienen un carácter metálico aún menor que los del grupo del boro, y suelen formar compuestos covalentes en lugar de iones positivos.
Grupo 15: Los elementos del grupo del nitrógeno
En el grupo 15 de la tabla periódica se encuentran los elementos del grupo del nitrógeno, que tienen un carácter metálico aún menor que los del grupo del carbono. Estos elementos tienen una electronegatividad alta y una energía de ionización alta, lo que significa que tienen una fuerte tendencia a atraer electrones hacia sí mismos.
Grupo 16: Los calcógenos
En el grupo 16 de la tabla periódica se encuentran los calcógenos, que tienen un carácter metálico aún menor que los del grupo del nitrógeno. Estos elementos tienen una electronegatividad y una energía de ionización muy altas, lo que significa que tienen una fuerte tendencia a atraer electrones hacia sí mismos.
Grupo 17: Los halógenos
En el grupo 17 de la tabla periódica se encuentran los halógenos, que son los elementos más electronegativos y menos metálicos de la tabla periódica. Estos elementos tienen una energía de ionización muy alta y una fuerte tendencia a atraer electrones hacia sí mismos, lo que los hace muy reactivos.
Grupo 18: Los gases nobles
En el grupo 18 de la tabla periódica se encuentran los gases nobles, que son los elementos menos reactivos y menos metálicos de la tabla periódica. Estos elementos tienen una electronegatividad muy baja y una energía de ionización muy alta, lo que significa que tienen una muy baja tendencia a ceder o atraer electrones.
Conclusión
El carácter metálico es una propiedad importante de los elementos que nos permite entender su comportamiento químico. En general, el carácter metálico varía de derecha a izquierda en un período y de abajo hacia arriba en un grupo de la tabla periódica. Los metales tienen un carácter metálico alto, lo que significa que tienen una fuerte tendencia a ceder electrones, mientras que los no metales tienen un carácter metálico bajo y
Deja una respuesta