¡Descubre la ley de conservación de la masa y su importancia!
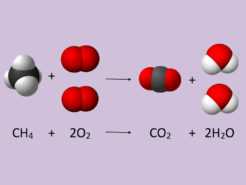
La ley de conservación de la masa es una de las leyes fundamentales de la química. Esta ley establece que en una reacción química, la masa total de los productos es igual a la masa total de los reactivos. Esto significa que la masa se conserva durante una reacción química, es decir, que no se crea ni se destruye materia durante una reacción química, sino que simplemente se transforma de una forma a otra.
Esta ley fue propuesta por el químico francés Antoine Lavoisier en el siglo XVIII. Lavoisier realizó un gran número de experimentos para demostrar la ley de conservación de la masa y fue uno de los primeros científicos en utilizar una balanza para medir la masa de los reactivos y productos en una reacción química.
La ley de conservación de la masa es importante en la química porque nos permite predecir la cantidad de productos que se obtendrán en una reacción química. Si conocemos la masa de los reactivos, podemos calcular la masa de los productos que se obtendrán. Además, esta ley nos permite entender cómo ocurren las reacciones químicas y cómo se transforman los elementos y compuestos durante estas reacciones.
La ley de conservación de la masa también es importante en la industria química y en la vida cotidiana. Por ejemplo, los fabricantes de alimentos y medicamentos deben seguir esta ley para garantizar que los productos que producen sean seguros y efectivos. Además, la ley de conservación de la masa se utiliza en la producción de materiales como plásticos, textiles y metales.
La ley de conservación de la masa es una ley fundamental de la química que establece que la masa se conserva durante una reacción química. Esta ley es importante porque nos permite predecir la cantidad de productos que se obtendrán en una reacción química y nos ayuda a entender cómo se transforman los elementos y compuestos durante estas reacciones. Además, esta ley es importante en la industria química y en la vida cotidiana.
- ¿Cómo se aplica la ley de conservación de la masa?
- ¿Por qué es importante balancear una ecuación química?
- ¿Cómo se puede demostrar la ley de conservación de la masa en un experimento?
- ¿Cómo se relaciona la ley de conservación de la masa con la ley de conservación de la energía?
- ¿Por qué es importante entender la ley de conservación de la masa?
¿Cómo se aplica la ley de conservación de la masa?
La ley de conservación de la masa se aplica en la química a través de ecuaciones químicas. En una ecuación química, se escriben los reactivos a la izquierda de la flecha y los productos a la derecha de la flecha. La ecuación química debe estar balanceada para que se cumpla la ley de conservación de la masa. Esto significa que la cantidad de átomos de cada elemento debe ser la misma en ambos lados de la ecuación.
Por ejemplo, la ecuación química para la reacción entre el hidrógeno y el oxígeno para formar agua es:
2H2 + O2 → 2H2O
En esta ecuación, hay cuatro átomos de hidrógeno y dos átomos de oxígeno en los reactivos. En los productos, hay cuatro átomos de hidrógeno y dos átomos de oxígeno. La ecuación está balanceada y cumple la ley de conservación de la masa.
¿Por qué es importante balancear una ecuación química?
Es importante balancear una ecuación química para que se cumpla la ley de conservación de la masa. Si la ecuación no está balanceada, la cantidad de átomos de cada elemento no será la misma en ambos lados de la ecuación y no se conservará la masa. Además, una ecuación química balanceada nos permite predecir la cantidad de productos que se obtendrán en una reacción química.
¿Cómo se puede demostrar la ley de conservación de la masa en un experimento?
Se puede demostrar la ley de conservación de la masa en un experimento utilizando una balanza. Para demostrar la ley de conservación de la masa, se debe medir la masa de los reactivos antes de una reacción química y la masa de los productos después de la reacción química. Si se cumple la ley de conservación de la masa, la masa total de los productos será igual a la masa total de los reactivos.
¿Cómo se relaciona la ley de conservación de la masa con la ley de conservación de la energía?
La ley de conservación de la masa y la ley de conservación de la energía son dos leyes fundamentales de la física y la química. La ley de conservación de la masa establece que la masa se conserva durante una reacción química, mientras que la ley de conservación de la energía establece que la energía se conserva durante una reacción química. Estas dos leyes están relacionadas porque la energía también se transforma durante una reacción química y la cantidad total de energía antes y después de la reacción química es la misma.
¿Por qué es importante entender la ley de conservación de la masa?
Es importante entender la ley de conservación de la masa porque nos permite predecir la cantidad de productos que se obtendrán en una reacción química y nos ayuda a entender cómo se transforman los elementos y compuestos durante estas reacciones. Además, esta ley es importante en la industria química y en la vida cotidiana. Los fabricantes de alimentos y medicamentos deben seguir esta ley para garantizar que los productos que producen sean seguros y efectivos. Además, la ley de conservación de la masa se utiliza en la producción de materiales como plásticos, textiles y metales.
Deja una respuesta