Descubre la estructura de Lewis: clave para entender la química
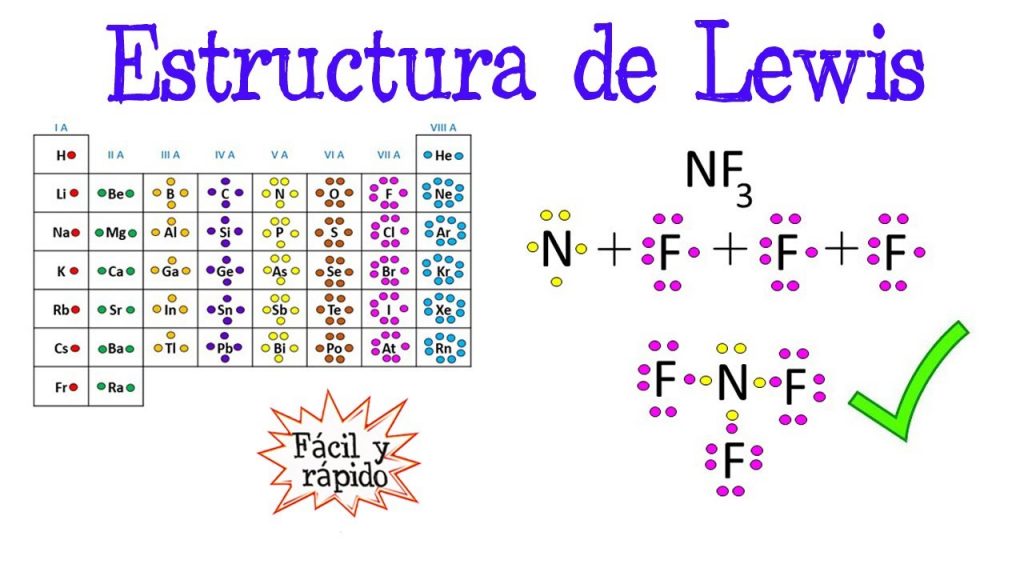
La química es una disciplina fundamental que nos permite entender cómo interactúan los elementos y compuestos en nuestro mundo. Una de las herramientas más importantes para entender la química es la estructura de Lewis, que nos permite visualizar cómo los átomos se unen y comparten electrones para formar moléculas. En este artículo, exploraremos la estructura de Lewis y cómo se utiliza en la química.
- ¿Qué es la estructura de Lewis?
- ¿Cómo se dibuja una estructura de Lewis?
- ¿Qué información nos proporciona la estructura de Lewis?
- ¿Cómo se utiliza la estructura de Lewis en la química?
- ¿Qué es la regla del octeto?
- ¿Cómo se determina la polaridad de una molécula a partir de la estructura de Lewis?
- Conclusión
- Preguntas frecuentes
¿Qué es la estructura de Lewis?
La estructura de Lewis es una representación gráfica de la estructura molecular de un compuesto químico. Fue desarrollada por el químico estadounidense Gilbert N. Lewis en 1916 como una forma de visualizar cómo los átomos interactúan entre sí para formar moléculas. La estructura de Lewis muestra los átomos como símbolos y los electrones que los rodean como puntos.
¿Cómo se dibuja una estructura de Lewis?
Para dibujar una estructura de Lewis, primero debemos conocer el número de electrones de valencia de cada átomo en la molécula. Los electrones de valencia son los electrones en la capa más externa de un átomo y son los que participan en las reacciones químicas. Luego, dibujamos los símbolos de los átomos y los rodeamos con puntos que representan los electrones de valencia. Los electrones se distribuyen de manera que cada átomo tenga ocho electrones en su capa de valencia (excepto el hidrógeno, que solo necesita dos electrones en su capa de valencia).
¿Qué información nos proporciona la estructura de Lewis?
La estructura de Lewis nos proporciona información valiosa sobre la forma en que los átomos se unen y comparten electrones para formar moléculas. Nos permite predecir la geometría molecular y la polaridad de una molécula, lo que a su vez nos ayuda a entender cómo interactúa con otras moléculas y reactivos.
¿Cómo se utiliza la estructura de Lewis en la química?
La estructura de Lewis se utiliza en la química para predecir la reactividad y las propiedades de las moléculas. También se utiliza para entender cómo se forman y rompen los enlaces químicos en las reacciones químicas. La estructura de Lewis es especialmente importante en la química orgánica, donde se utiliza para predecir la estructura y reactividad de los compuestos orgánicos.
¿Qué es la regla del octeto?
La regla del octeto es una regla empírica que establece que los átomos tienden a ganar, perder o compartir electrones hasta que tengan ocho electrones en su capa de valencia. Esto se debe a que los átomos con ocho electrones en su capa de valencia están en un estado de energía más estable, similar al de los gases nobles. La regla del octeto es útil para predecir la estructura de Lewis de una molécula y la forma en que se unen los átomos.
¿Cómo se determina la polaridad de una molécula a partir de la estructura de Lewis?
La polaridad de una molécula se determina a partir de la estructura de Lewis a través de la distribución de cargas eléctricas en la molécula. Si una molécula tiene una distribución de carga desigual, es decir, si hay una región con carga positiva y otra con carga negativa, se dice que la molécula es polar. Si la distribución de carga es uniforme, la molécula es no polar. La polaridad de una molécula es importante porque afecta cómo interactúa con otras moléculas y con los campos eléctricos.
Conclusión
La estructura de Lewis es una herramienta clave para entender la química y cómo los átomos se unen para formar moléculas. Nos permite visualizar los electrones de valencia de los átomos y predecir la geometría molecular y la polaridad de una molécula. La estructura de Lewis se utiliza ampliamente en la química para predecir la reactividad y las propiedades de las moléculas y es especialmente importante en la química orgánica.
Preguntas frecuentes
¿Pueden los átomos tener más de ocho electrones en su capa de valencia?
Sí, algunos átomos pueden tener más de ocho electrones en su capa de valencia, especialmente aquellos con orbitales d y f. Esto se conoce como la regla del octeto extendido.
¿Qué es una molécula no polar?
Una molécula no polar es una molécula en la que la distribución de carga eléctrica es uniforme y no hay regiones con carga positiva o negativa.
¿Qué es un enlace covalente?
Un enlace covalente es un tipo de enlace químico en el que dos átomos comparten un par de electrones en su capa de valencia.
¿Por qué es importante la polaridad de una molécula?
La polaridad de una molécula es importante porque afecta cómo interactúa con otras moléculas y con los campos eléctricos. La polaridad también puede afectar la solubilidad de una molécula en diferentes solventes.
¿Qué es la geometría molecular?
La geometría molecular es la disposición tridimensional de los átomos en una molécula. La geometría molecular está determinada por la estructura de Lewis y afecta las propiedades y reactividad de la molécula.
Deja una respuesta