Descubre la estructura de la tabla periódica en detalle
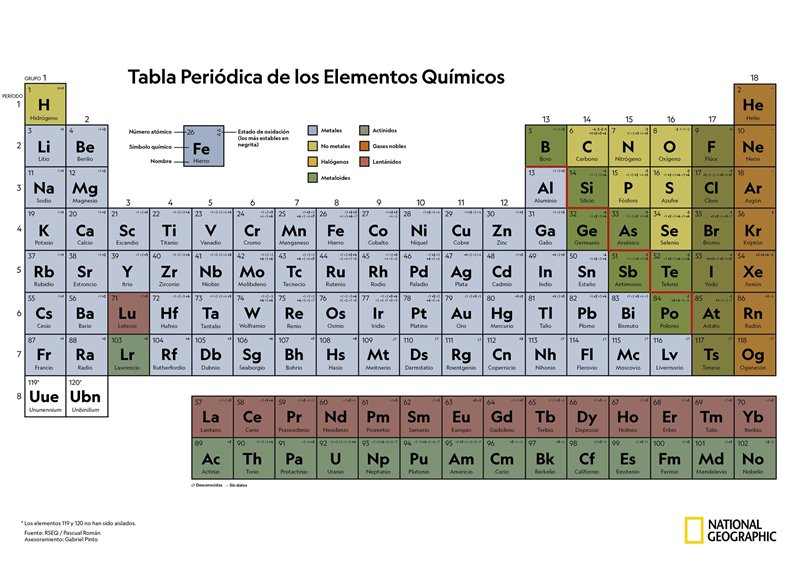
La tabla periódica es una herramienta esencial en la química y es crucial para la comprensión de los elementos y sus propiedades. Desde su creación en 1869 por el químico ruso Dmitri Mendeléyev, la tabla periódica ha evolucionado para incluir los 118 elementos conocidos actualmente. En este artículo, vamos a explorar la estructura de la tabla periódica en detalle.
La estructura básica de la tabla periódica
La tabla periódica se organiza en filas horizontales llamadas períodos y columnas verticales llamadas grupos. Los elementos se colocan en la tabla periódica en orden creciente de su número atómico, que es el número de protones en el núcleo de un átomo. Los elementos en la misma columna tienen propiedades similares porque tienen la misma cantidad de electrones en su capa externa.
Grupos de la tabla periódica
Los grupos de la tabla periódica se numeran del 1 al 18. Los elementos en el Grupo 1 se llaman metales alcalinos y son altamente reactivos porque tienen un solo electrón en su capa externa. Los elementos en el Grupo 2 se llaman metales alcalinotérreos y también son altamente reactivos debido a sus dos electrones en la capa externa.
Los elementos en el Grupo 17 se llaman halógenos y son altamente reactivos porque tienen siete electrones en su capa externa. Los elementos en el Grupo 18 se llaman gases nobles y son muy estables porque tienen una capa externa completa de electrones.
Períodos de la tabla periódica
Los períodos de la tabla periódica se numeran del 1 al 7. Los elementos en el mismo período tienen la misma cantidad de capas electrónicas. A medida que se mueve de izquierda a derecha en un período, el número atómico aumenta y las propiedades químicas de los elementos cambian.
La tabla periódica extendida
La tabla periódica original de Mendeléyev tenía 63 elementos. Desde entonces, se han descubierto y sintetizado muchos más elementos, llevando la tabla periódica a contener 118 elementos. La tabla periódica extendida también incluye información adicional sobre los elementos, como sus estados de oxidación, electronegatividades y radios atómicos.
Elementos de transición
Los elementos de transición se encuentran en los grupos 3 a 12 de la tabla periódica y son conocidos por sus propiedades de transición entre los metales y no metales. Estos elementos tienen una capa externa incompleta y pueden tener múltiples estados de oxidación.
Lantánidos y actínidos
Los lantánidos y actínidos son dos series de elementos que se ubican debajo de la tabla periódica principal. Los lantánidos son los 15 elementos que comienzan con lantano (La) y terminan en lutecio (Lu). Los actínidos son los 15 elementos que comienzan con actinio (Ac) y terminan en lawrencio (Lr). Estos elementos son conocidos por sus propiedades radiactivas y se utilizan para la energía nuclear.
Conclusion
La tabla periódica es una herramienta esencial para la química y la ciencia en general. La estructura básica de la tabla periódica se compone de grupos y períodos, y los elementos se organizan en orden creciente de número atómico. La tabla periódica extendida incluye información adicional sobre los elementos, como sus estados de oxidación y radios atómicos. Los elementos de transición y las series lantánidos y actínidos son importantes para la química y la energía nuclear.
Preguntas frecuentes
¿Cómo se organizan los elementos en la tabla periódica?
Los elementos se organizan en la tabla periódica en orden creciente de número atómico. Los elementos en la misma columna tienen propiedades similares porque tienen la misma cantidad de electrones en su capa externa.
¿Qué son los grupos y períodos en la tabla periódica?
Los grupos son columnas verticales en la tabla periódica, mientras que los períodos son filas horizontales. Los elementos en el mismo grupo tienen propiedades similares porque tienen la misma cantidad de electrones en su capa externa. Los elementos en el mismo período tienen la misma cantidad de capas electrónicas.
¿Qué son los elementos de transición?
Los elementos de transición se encuentran en los grupos 3 a 12 de la tabla periódica y son conocidos por sus propiedades de transición entre los metales y no metales. Estos elementos tienen una capa externa incompleta y pueden tener múltiples estados de oxidación.
¿Qué son los lantánidos y actínidos?
Los lantánidos y actínidos son dos series de elementos que se ubican debajo de la tabla periódica principal. Los lantánidos son los 15 elementos que comienzan con lantano (La) y terminan en lutecio (Lu). Los actínidos son los 15 elementos que comienzan con actinio (Ac) y terminan en lawrencio (Lr). Estos elementos son conocidos por sus propiedades radiactivas y se utilizan para la energía nuclear.
¿Por qué es importante la tabla periódica?
La tabla periódica es importante para la química y la ciencia en general porque nos ayuda a entender los elementos y sus propiedades. La tabla periódica también se utiliza como herramienta para la predicción de reacciones químicas y la síntesis de nuevos compuestos.
Deja una respuesta