Descubre la estructura atómica: Electrones en la tabla periódica
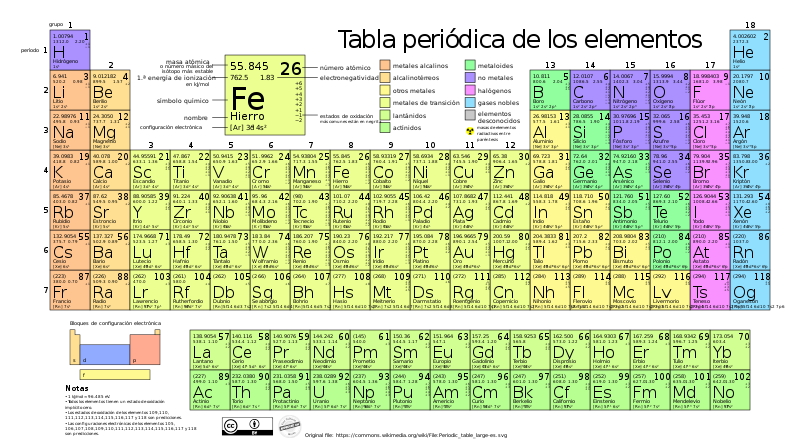
La tabla periódica es una herramienta esencial para comprender la estructura de los átomos y cómo se combinan para formar moléculas y compuestos. En su interior, se encuentra información detallada sobre los elementos químicos, incluyendo su número atómico, peso atómico y configuración electrónica. En este artículo, exploraremos la estructura atómica y cómo los electrones se organizan en la tabla periódica.
¿Qué es un átomo?
Un átomo es la unidad básica de la materia. Está compuesto por un núcleo central que contiene protones y neutrones, y una nube de electrones que orbitan alrededor del núcleo. El número de protones en el núcleo determina el número atómico del elemento y su posición en la tabla periódica.
¿Qué son los electrones?
Los electrones son partículas subatómicas con carga negativa que orbitan alrededor del núcleo en capas o niveles de energía. En la tabla periódica, los elementos están organizados en filas y columnas según su configuración electrónica. Los electrones son responsables de las propiedades químicas de los elementos, incluyendo su capacidad para formar enlaces y reaccionar con otros elementos.
Configuración electrónica
La configuración electrónica es la distribución de electrones en los diferentes niveles de energía alrededor del núcleo. Los niveles de energía se numeran del 1 al 7, comenzando por el nivel más cercano al núcleo. El número máximo de electrones que puede contener cada nivel de energía se calcula utilizando la fórmula 2n², donde n es el número del nivel de energía.
Por ejemplo, el nivel 1 puede contener un máximo de 2 electrones (2 x 1² = 2), el nivel 2 puede contener un máximo de 8 electrones (2 x 2² = 8) y el nivel 3 puede contener un máximo de 18 electrones (2 x 3² = 18).
Regla del octeto
La regla del octeto establece que los átomos tienden a ganar, perder o compartir electrones para alcanzar una configuración electrónica estable con ocho electrones en su capa más externa. Esta regla explica por qué algunos elementos tienden a formar iones cargados positiva o negativamente, mientras que otros tienden a formar enlaces covalentes compartiendo electrones con otros átomos.
Electrones en la tabla periódica
La tabla periódica se organiza en filas llamadas periodos y columnas llamadas grupos. Los elementos en el mismo grupo tienen la misma configuración electrónica en su capa más externa, lo que les da propiedades químicas similares. Por ejemplo, los elementos del grupo 1, conocidos como metales alcalinos, tienen un solo electrón en su capa más externa y tienden a perder ese electrón para formar iones positivos.
Los elementos en el mismo periodo tienen el mismo número de niveles de energía y la cantidad de electrones en su capa más externa aumenta de izquierda a derecha en la tabla periódica. Por ejemplo, el hidrógeno y el helio están en el primer periodo y tienen un y dos electrones en su capa más externa, respectivamente. A medida que avanzamos hacia la derecha en el periodo, los elementos tienen más electrones en su capa más externa, lo que los hace menos reactivos.
Tabla periódica de los elementos
A continuación, se presenta una tabla periódica de los elementos con información sobre su número atómico, peso atómico y configuración electrónica.
| Elemento | Número atómico | Peso atómico | Configuración electrónica |
|---|---|---|---|
| Hidrógeno | 1 | 1.008 | 1s¹ |
| Helio | 2 | 4.003 | 1s² |
| Litio | 3 | 6.941 | 1s² 2s¹ |
| Berilio | 4 | 9.012 | 1s² 2s² |
| Boro | 5 | 10.81 | 1s² 2s² 2p¹ |
| Carbono | 6 | 12.01 | 1s² 2s² 2p² |
| Nitrógeno | 7 | 14.01 | 1s² 2s² 2p³ |
| Oxígeno | 8 | 16.00 | 1s² 2s² 2p⁴ |
| Flúor | 9 | 19.00 | 1s² 2s² 2p⁵ |
| Neón | 10 | 20.18 | 1s² 2s² 2p⁶ |
Conclusión
La tabla periódica es una herramienta esencial para comprender la estructura atómica y cómo los electrones se organizan en los diferentes elementos químicos. La configuración electrónica de un átomo determina sus propiedades químicas y su capacidad para formar enlaces con otros átomos. Al comprender la estructura atómica y la tabla periódica, podemos predecir cómo los elementos interactuarán y cómo se formarán los compuestos químicos.
Preguntas frecuentes
1. ¿Cómo se organizan los elementos en la tabla periódica?
Los elementos se organizan en filas llamadas periodos y columnas llamadas grupos. Los elementos en el mismo grupo tienen la misma configuración electrónica en su capa más externa, lo que les da propiedades químicas similares. Los elementos en el mismo periodo tienen el mismo número de niveles de energía.
2. ¿Qué es la configuración electrónica?
La configuración electrónica es la distribución de electrones en los diferentes nive
Deja una respuesta