Descubre el significado del número atómico y de masa en la química
En el mundo de la química, hay dos términos que son cruciales para entender la estructura de los átomos: el número atómico y la masa atómica. Estos dos términos están íntimamente relacionados entre sí, pero a menudo son confundidos por los estudiantes de química. En este artículo, vamos a explorar el significado de cada uno de ellos y cómo están relacionados.
¿Qué es el número atómico?
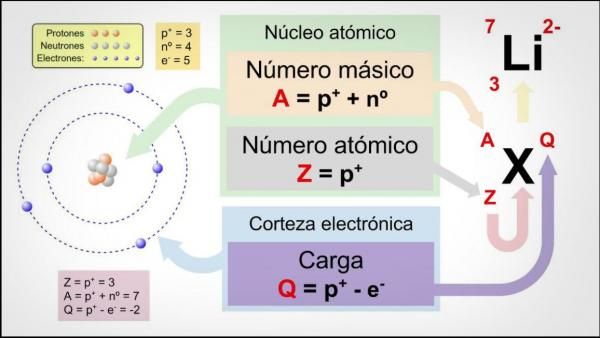
El número atómico es el número de protones que se encuentran en el núcleo de un átomo. Los protones tienen una carga positiva y son uno de los dos tipos de partículas que se encuentran en el núcleo de un átomo. El número atómico se representa con la letra Z y es un número entero que es único para cada elemento químico en la tabla periódica.
Por ejemplo, el número atómico del hidrógeno es 1, lo que significa que hay un solo protón en el núcleo de un átomo de hidrógeno. El número atómico del helio es 2, lo que significa que hay dos protones en el núcleo de un átomo de helio.
¿Qué es la masa atómica?
La masa atómica es la masa total de un átomo. Está compuesta por la masa de los protones, los neutrones y los electrones que se encuentran en el átomo. Los protones y los neutrones se encuentran en el núcleo del átomo, mientras que los electrones orbitan alrededor del núcleo en capas llamadas niveles de energía.
La masa atómica se representa con la letra A y se expresa en unidades de masa atómica (uma). Una unidad de masa atómica es igual a la masa de un átomo de carbono-12, que se define como 12 uma. Por lo tanto, la masa atómica de cualquier elemento es un número que indica cuántas veces la masa de un átomo de ese elemento es mayor que la masa de un átomo de carbono-12.
Por ejemplo, la masa atómica del hidrógeno es aproximadamente 1 uma, lo que significa que la masa de un átomo de hidrógeno es aproximadamente una doceava parte de la masa de un átomo de carbono-12. La masa atómica del helio es de aproximadamente 4 uma, lo que significa que la masa de un átomo de helio es cuatro veces mayor que la masa de un átomo de carbono-12.
Relación entre número atómico y masa atómica
El número atómico y la masa atómica están relacionados entre sí de la siguiente manera: la masa atómica de un átomo es igual al número de protones y neutrones en el núcleo del átomo. Por lo tanto, la masa atómica de un elemento es aproximadamente igual a la suma de los protones y neutrones en el núcleo de un átomo de ese elemento.
Por ejemplo, el isótopo más común del carbono tiene un número atómico de 6 y una masa atómica de aproximadamente 12 uma. Esto significa que el átomo de carbono tiene seis protones y seis neutrones en su núcleo.
Tabla periódica y número atómico
El número atómico es un número único para cada elemento químico y es la base para la organización de la tabla periódica. La tabla periódica enumera los elementos en orden creciente de número atómico, lo que significa que los elementos con números atómicos más bajos se encuentran en la parte superior de la tabla y los elementos con números atómicos más altos se encuentran en la parte inferior.
Además, el número atómico también determina la posición de un elemento en la tabla periódica. Los elementos con números atómicos similares tienen propiedades químicas similares y se encuentran en grupos verticales en la tabla periódica.
Conclusión
El número atómico y la masa atómica son dos conceptos fundamentales en la química que están íntimamente relacionados entre sí. El número atómico es el número de protones que se encuentran en el núcleo de un átomo, mientras que la masa atómica es la masa total de un átomo. La masa atómica está determinada por el número de protones y neutrones en el núcleo del átomo. Además, el número atómico es la base para la organización de la tabla periódica y determina la posición de los elementos en la tabla.
Preguntas frecuentes
1. ¿Por qué es importante entender el número atómico y la masa atómica?
Es importante entender el número atómico y la masa atómica porque son conceptos fundamentales en la química y son cruciales para entender la estructura de los átomos y la organización de la tabla periódica.
2. ¿Por qué es importante la organización de la tabla periódica?
La organización de la tabla periódica es importante porque permite a los científicos predecir las propiedades químicas de los elementos y sus compuestos. Además, la tabla periódica es una herramienta útil para la identificación de elementos y su uso en aplicaciones prácticas.
3. ¿Qué es un isótopo?
Un isótopo es un átomo de un elemento que tiene el mismo número de protones pero un número diferente de neutrones en su núcleo. Esto significa que los isótopos de un elemento tienen la misma carga nuclear pero diferentes masas atómicas.
4. ¿Cómo se determina el número de protones en un átomo?
El número de protones en un átomo se determina por el número atómico del elemento. El número atómico es el número de protones que se encuentran en el núcleo de un átomo de un elemento determinado.
5. ¿Cuál es la diferencia entre masa atómica y peso atómico?
La masa atómica es la masa total de un átomo, mientras que el peso atómico es la masa promedio de todos los isótopos de un elemento. La masa atómica se expresa en unidades de masa atómica (uma), mientras que el peso atómico se expresa en unidades de masa atómica relativa (u).
Deja una respuesta