Descubre el carácter metálico: propiedades y definición
Los metales son elementos químicos que se caracterizan por su brillo, su conductividad térmica y eléctrica, su maleabilidad y su ductilidad. El carácter metálico es una propiedad que se refiere a la capacidad que tienen los elementos para perder electrones y formar cationes. En este artículo, exploraremos en detalle las propiedades y la definición del carácter metálico.
¿Qué es el carácter metálico?
El carácter metálico es una propiedad de los elementos químicos que se refiere a su capacidad para perder electrones y formar cationes. Los elementos con un alto carácter metálico tienden a tener baja energía de ionización y baja afinidad electrónica, lo que significa que es fácil para ellos liberar electrones y formar iones positivos.
Propiedades del carácter metálico
Entre las principales propiedades del carácter metálico, se encuentran las siguientes:
Brillo metálico
Los metales tienen un brillo característico, llamado brillo metálico, que se debe a su capacidad para reflejar la luz. Este brillo se debe a la forma en la que los electrones en los metales interactúan con la luz.
Conductividad térmica y eléctrica
Los metales son excelentes conductores de calor y electricidad. Esto se debe a la forma en que los electrones se mueven en los metales, lo que permite que la energía se transfiera fácilmente a través del material.
Maleabilidad y ductilidad
Los metales son maleables y ductiles, lo que significa que se pueden deformar sin romperse y se pueden estirar en hilos finos. Esto se debe a la forma en que los átomos de metal se empaquetan juntos en una estructura cristalina.
Reactividad química
Los metales son generalmente reactivos químicamente, lo que significa que pueden reaccionar con otros elementos para formar compuestos. La reactividad de los metales varía según su posición en la tabla periódica.
Definición del carácter metálico
El carácter metálico se define como la capacidad de un elemento para perder electrones y formar cationes. Los elementos con un alto carácter metálico tienden a tener baja energía de ionización y baja afinidad electrónica, lo que significa que es fácil para ellos liberar electrones y formar iones positivos.
Tabla periódica y carácter metálico
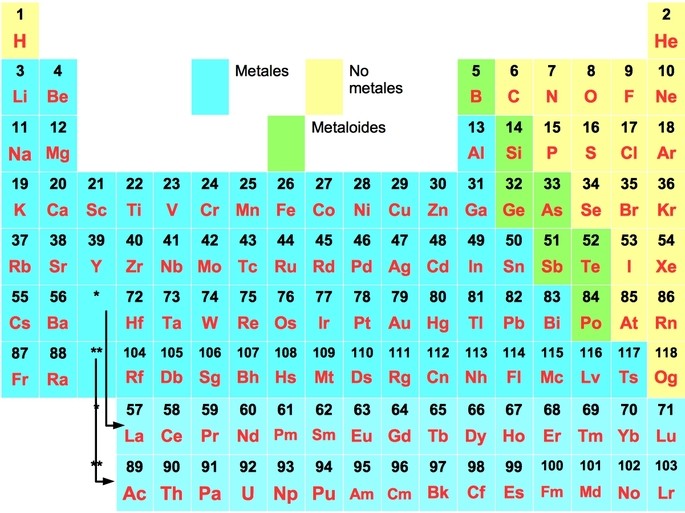
La tabla periódica de los elementos se organiza en función de las propiedades de los elementos, incluido el carácter metálico. En general, los metales se encuentran en la parte izquierda de la tabla periódica, mientras que los no metales se encuentran en la parte derecha. Los elementos con un alto carácter metálico se encuentran en la parte inferior izquierda de la tabla periódica, mientras que los elementos con un bajo carácter metálico se encuentran en la parte superior derecha.
Ejemplos de elementos con alto y bajo carácter metálico
Algunos ejemplos de elementos con alto carácter metálico incluyen el litio, el sodio y el potasio. Estos elementos tienen baja energía de ionización y baja afinidad electrónica, lo que significa que es fácil para ellos perder electrones y formar cationes.
Por otro lado, algunos ejemplos de elementos con bajo carácter metálico incluyen el flúor, el oxígeno y el nitrógeno. Estos elementos tienen alta energía de ionización y alta afinidad electrónica, lo que significa que es difícil para ellos perder electrones y formar cationes.
Conclusión
El carácter metálico es una propiedad importante de los elementos químicos que se refiere a su capacidad para perder electrones y formar cationes. Los metales tienen un alto carácter metálico y se caracterizan por su brillo, conductividad térmica y eléctrica, maleabilidad y ductilidad. La tabla periódica de los elementos se organiza en función del carácter metálico, con los metales en la parte izquierda y los no metales en la parte derecha.
Preguntas frecuentes
¿Qué es el brillo metálico?
El brillo metálico es un brillo característico que tienen los metales debido a su capacidad para reflejar la luz.
¿Por qué los metales son buenos conductores de calor y electricidad?
Los metales son buenos conductores de calor y electricidad debido a la forma en que los electrones se mueven en los metales, lo que permite que la energía se transfiera fácilmente a través del material.
¿Qué elementos tienen alto carácter metálico?
Algunos ejemplos de elementos con alto carácter metálico incluyen el litio, el sodio y el potasio.
¿Qué elementos tienen bajo carácter metálico?
Algunos ejemplos de elementos con bajo carácter metálico incluyen el flúor, el oxígeno y el nitrógeno.
¿Cómo se organiza la tabla periódica en función del carácter metálico?
La tabla periódica se organiza en función del carácter metálico, con los metales en la parte izquierda y los no metales en la parte derecha. Los elementos con un alto carácter metálico se encuentran en la parte inferior izquierda, mientras que los elementos con un bajo carácter metálico se encuentran en la parte superior derecha.
Deja una respuesta