Descubre el número de oxidación de cualquier elemento con estos pasos
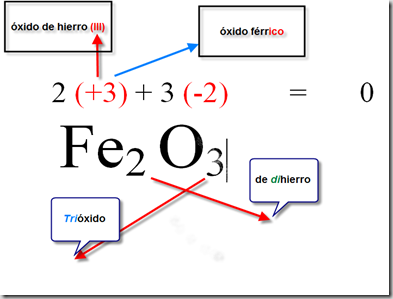
El número de oxidación es un concepto fundamental en la química, ya que nos permite entender cómo se combinan los elementos para formar compuestos. Además, es esencial para poder balancear ecuaciones químicas y predecir la reactividad de los elementos. En este artículo te explicaremos cómo puedes descubrir el número de oxidación de cualquier elemento con unos sencillos pasos.
¿Qué es el número de oxidación?
El número de oxidación es una medida del grado de pérdida o ganancia de electrones que experimenta un átomo al formar un compuesto. En otras palabras, es la carga eléctrica que tendría un átomo si todos sus enlaces fueran iónicos.
Por ejemplo, en el compuesto de cloruro de sodio (NaCl), el sodio tiene un número de oxidación de +1, mientras que el cloro tiene un número de oxidación de -1. Esto significa que el sodio ha perdido un electrón y el cloro lo ha ganado.
¿Cómo se determina el número de oxidación?
Existen varias reglas que te permiten determinar el número de oxidación de un elemento. Aquí te presentamos algunos pasos que puedes seguir:
Paso 1: Identifica el tipo de enlace
El número de oxidación depende del tipo de enlace que se forma entre los elementos. Si se trata de un enlace iónico, el número de oxidación se determina por la carga que tiene el ion. Si se trata de un enlace covalente, el número de oxidación se determina por la electronegatividad de cada elemento.
Paso 2: Identifica los elementos que participan en el enlace
Una vez que sabes el tipo de enlace, debes identificar los elementos que participan en él. Esto te permitirá conocer las cargas que tienen los iones o la electronegatividad de cada elemento.
Paso 3: Asigna el número de oxidación
Una vez que tienes la información necesaria, puedes asignar el número de oxidación siguiendo estas reglas:
- El número de oxidación de un elemento libre (sin combinarse con otros elementos) es siempre 0.
- El número de oxidación de un ion monoatómico es igual a la carga del ion.
- En un compuesto, el número de oxidación del elemento más electronegativo es negativo y el del elemento menos electronegativo es positivo.
- La suma de los números de oxidación de todos los elementos en un compuesto es igual a 0. En un ion, la suma de los números de oxidación es igual a la carga del ion.
Ejemplos de cómo determinar el número de oxidación
A continuación, te presentamos algunos ejemplos para que puedas entender mejor cómo se determina el número de oxidación:
Ejemplo 1: Cloruro de sodio (NaCl)
- Tipo de enlace: iónico
- Elementos involucrados: sodio (Na) y cloro (Cl)
- Carga del ion: Na+ y Cl-
- Número de oxidación: Na = +1, Cl = -1
Ejemplo 2: Agua (H2O)
- Tipo de enlace: covalente
- Elementos involucrados: hidrógeno (H) y oxígeno (O)
- Electronegatividad: H = 2,1 y O = 3,5
- Número de oxidación: H = +1, O = -2
Ejemplo 3: Dióxido de carbono (CO2)
- Tipo de enlace: covalente
- Elementos involucrados: carbono (C) y oxígeno (O)
- Electronegatividad: C = 2,5 y O = 3,5
- Número de oxidación: C = +4, O = -2
Conclusión
El número de oxidación es un concepto fundamental en la química, ya que nos permite entender cómo se combinan los elementos para formar compuestos. Aunque puede parecer complicado determinar el número de oxidación, siguiendo los pasos que te hemos presentado podrás hacerlo con facilidad. Recuerda que el número de oxidación es esencial para poder balancear ecuaciones químicas y predecir la reactividad de los elementos.
Preguntas frecuentes
1. ¿Qué es el número de oxidación?
El número de oxidación es una medida del grado de pérdida o ganancia de electrones que experimenta un átomo al formar un compuesto.
2. ¿Cómo se determina el número de oxidación?
El número de oxidación se determina siguiendo algunas reglas, dependiendo del tipo de enlace y los elementos involucrados.
3. ¿Por qué es importante el número de oxidación?
El número de oxidación es importante porque nos permite entender cómo se combinan los elementos para formar compuestos, balancear ecuaciones químicas y predecir la reactividad de los elementos.
4. ¿Qué es un enlace iónico?
Un enlace iónico es un tipo de enlace químico que se forma entre elementos con diferencias grandes de electronegatividad, y que se caracteriza por la transferencia de electrones.
5. ¿Qué es un enlace covalente?
Un enlace covalente es un tipo de enlace químico que se forma entre elementos con diferencias pequeñas de electronegatividad, y que se caracteriza por el compartimiento de electrones.
Deja una respuesta