Calcula los gramos de soluto en tu solución de forma sencilla
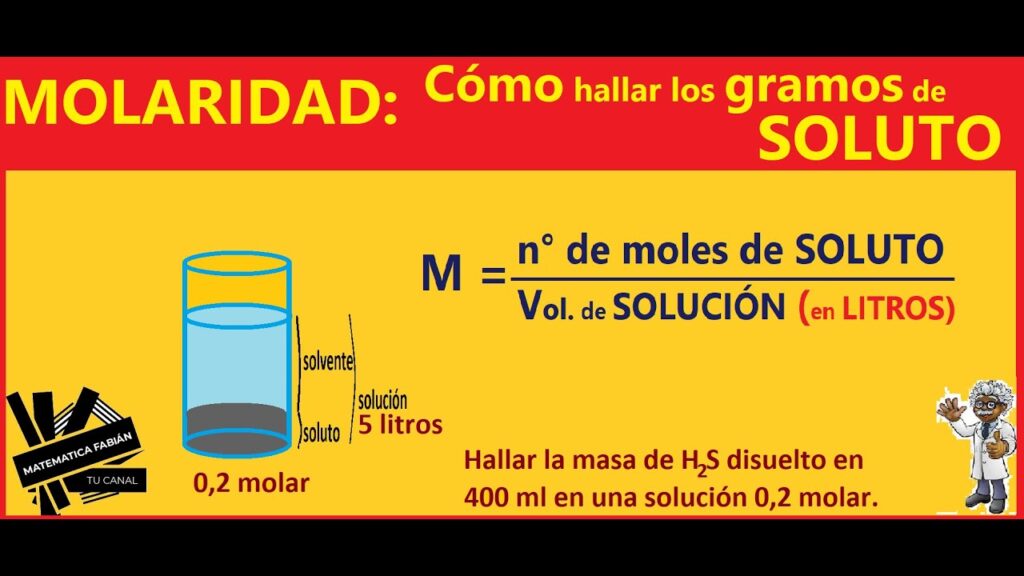
¿Te has preguntado alguna vez cuántos gramos de soluto hay en tu solución? Saber esto es fundamental para poder realizar cálculos y ajustar la concentración de la solución según tus necesidades.
En este artículo te explicaremos cómo calcular los gramos de soluto en tu solución de forma sencilla y práctica, utilizando diferentes métodos y herramientas.
¿Qué es un soluto?
Antes de empezar, es importante entender qué es un soluto. Un soluto es una sustancia que se disuelve en otra sustancia, llamada solvente, para formar una solución. Por ejemplo, si disolvemos azúcar en agua, el azúcar es el soluto y el agua es el solvente.
¿Por qué es importante conocer la cantidad de soluto en una solución?
Conocer la cantidad de soluto en una solución es importante por varias razones:
- Permite calcular la concentración de la solución.
- Permite ajustar la concentración de la solución según nuestras necesidades.
- Es útil para realizar cálculos en química y otras áreas de la ciencia.
Cómo calcular los gramos de soluto en una solución
Existen diferentes métodos y herramientas para calcular los gramos de soluto en una solución. A continuación, te explicamos algunos de los más comunes:
Método de la regla de tres
El método de la regla de tres es un método sencillo y práctico para calcular los gramos de soluto en una solución. Para utilizar este método, se deben conocer dos de las siguientes cantidades: la concentración de la solución, el volumen de la solución y la cantidad de soluto.
Por ejemplo, si tenemos una solución con una concentración de 0.5 M y un volumen de 250 mL, podemos calcular la cantidad de soluto de la siguiente manera:
1. Convertimos el volumen a litros: 250 mL = 0.25 L
2. Utilizamos la fórmula de la concentración: C = n/V, donde C es la concentración, n es la cantidad de soluto y V es el volumen. Despejando n, obtenemos: n = C x V.
3. Sustituimos los valores conocidos: n = 0.5 M x 0.25 L = 0.125 moles.
4. Utilizamos la masa molar del soluto para convertir moles a gramos. Por ejemplo, si el soluto es NaCl, su masa molar es de 58.44 g/mol. Entonces, la cantidad de soluto en gramos es: 0.125 moles x 58.44 g/mol = 7.3 g.
Método del factor de conversión
El método del factor de conversión es similar al método de la regla de tres, pero utiliza un factor de conversión para convertir unidades. Por ejemplo, si queremos convertir una concentración en g/L a moles/L, podemos utilizar el factor de conversión de la masa molar.
Por ejemplo, si tenemos una solución con una concentración de 2 g/L de NaCl, podemos calcular la cantidad de soluto de la siguiente manera:
1. Utilizamos el factor de conversión de la masa molar: 1 mol de NaCl = 58.44 g de NaCl.
2. Convertimos la concentración a moles/L: 2 g/L / 58.44 g/mol = 0.034 moles/L.
3. Multiplicamos la concentración en moles/L por el volumen de la solución en litros para obtener la cantidad de soluto en moles: 0.034 moles/L x 0.5 L = 0.017 moles.
4. Multiplicamos la cantidad de soluto en moles por la masa molar del soluto para obtener la cantidad de soluto en gramos: 0.017 moles x 58.44 g/mol = 0.99 g.
Calculadora de concentración
Existen calculadoras de concentración en línea que permiten calcular los gramos de soluto en una solución de forma rápida y sencilla. Estas calculadoras suelen requerir que se introduzcan los valores de la concentración, el volumen y la masa molar del soluto.
Preguntas frecuentes
¿Qué es la concentración de una solución?
La concentración de una solución es la cantidad de soluto que hay en una cantidad determinada de solvente o solución. Se expresa en unidades de masa por volumen o moles por volumen, entre otras.
¿Qué es la masa molar?
La masa molar es la masa de un mol de una sustancia. Se expresa en unidades de gramos por mol.
¿Qué es la regla de tres?
La regla de tres es un método matemático que permite calcular una cantidad a partir de otras dos cantidades conocidas. Se utiliza frecuentemente en problemas de proporciones y porcentajes.
¿Qué es un mol?
Un mol es una unidad de medida utilizada en química para expresar la cantidad de sustancia. Un mol de una sustancia contiene una cantidad determinada de partículas, que depende del tipo de sustancia.
¿Qué es una solución?
Una solución es una mezcla homogénea de dos o más sustancias, donde una de ellas, llamada soluto, se encuentra disuelta en otra, llamada solvente.
Deja una respuesta