Aprende a resolver problemas de calorimetría con este esquema
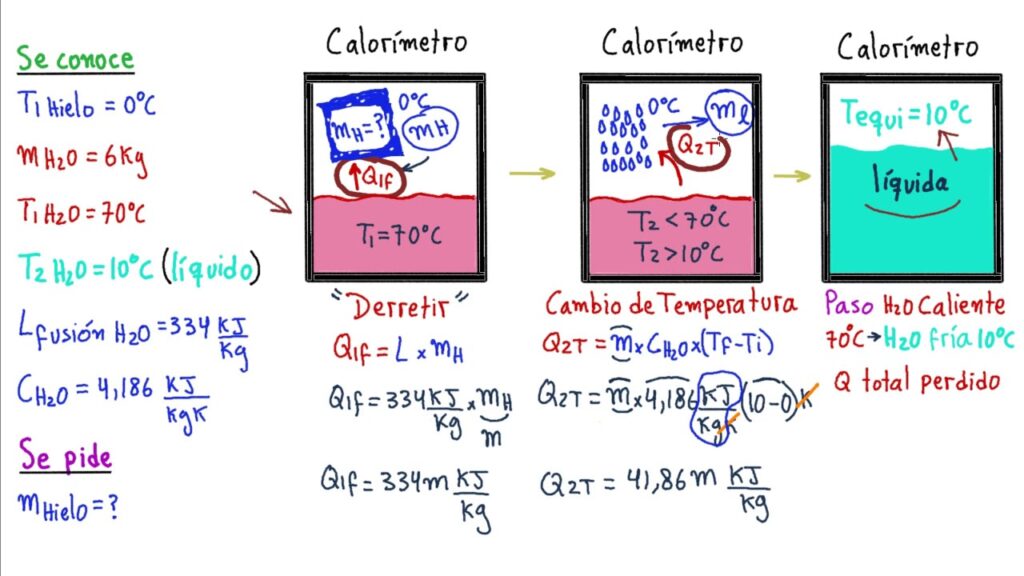
La calorimetría es una rama de la física que se encarga de estudiar las transferencias de calor entre sistemas. Algunos ejemplos de situaciones en las que se aplica la calorimetría son el estudio del cambio de temperatura de un cuerpo al recibir o ceder calor, o la determinación de la cantidad de calor necesaria para llevar a cabo una reacción química.
En la resolución de problemas de calorimetría, es importante tener en cuenta los conceptos fundamentales que rigen estas transferencias de calor. Para ello, podemos utilizar un esquema que nos ayudará a visualizar de forma clara y ordenada los datos y las incógnitas del problema.
A continuación, te presentamos un esquema que te guiará en la resolución de problemas de calorimetría:
- Paso 1: Identificar los datos del problema
- Paso 2: Identificar las incógnitas del problema
- Paso 3: Aplicar la ley de conservación de la energía
- Paso 4: Resolver la ecuación y obtener la solución
- Conclusión
- Preguntas frecuentes
- 1. ¿Qué es la capacidad calorífica?
- 2. ¿Qué es la ley de conservación de la energía?
- 3. ¿Cómo se calcula la cantidad de calor que se transfiere entre dos cuerpos?
- 4. ¿Por qué es importante aplicar la ley de conservación de la energía en la resolución de problemas de calorimetría?
- 5. ¿Qué otros conceptos están relacionados con la calorimetría?
Paso 1: Identificar los datos del problema
Lo primero que debemos hacer es leer el enunciado del problema y extraer la información relevante. En la mayoría de los casos, esta información se presenta en forma de datos numéricos y unidades de medida.
Ejemplo:
Un recipiente de 500 gramos de agua a 20°C se mezcla con 300 gramos de agua a 40°C. ¿Cuál será la temperatura final de la mezcla?
En este caso, los datos que podemos identificar son:
- Masa del primer cuerpo (m1): 500 gramos
- Temperatura inicial del primer cuerpo (T1): 20°C
- Masa del segundo cuerpo (m2): 300 gramos
- Temperatura inicial del segundo cuerpo (T2): 40°C
- Temperatura final de la mezcla (Tf): ¿?
Paso 2: Identificar las incógnitas del problema
Una vez que hemos identificado los datos del problema, debemos determinar qué es lo que se nos pide calcular. En la mayoría de los casos, la incógnita estará relacionada con la temperatura final de la mezcla o con la cantidad de calor que se ha transferido entre los cuerpos.
Ejemplo:
En el problema anterior, la incógnita es la temperatura final de la mezcla (Tf).
Paso 3: Aplicar la ley de conservación de la energía
La ley de conservación de la energía establece que la energía no se crea ni se destruye, sino que se transforma de una forma a otra. En el caso de las transferencias de calor, esto significa que la cantidad de calor que pierde un cuerpo es igual a la cantidad de calor que gana el otro cuerpo.
Ejemplo:
En el problema anterior, podemos aplicar la ley de conservación de la energía de la siguiente forma:
- El primer cuerpo pierde una cantidad de calor (Q1) que se calcula con la fórmula Q1 = m1 * c * (T1 - Tf), donde c es la capacidad calorífica del agua (1 cal/g·°C).
- El segundo cuerpo gana una cantidad de calor (Q2) que se calcula con la fórmula Q2 = m2 * c * (Tf - T2).
- Como la cantidad de calor que pierde el primer cuerpo es igual a la cantidad de calor que gana el segundo cuerpo, podemos igualar estas dos ecuaciones y despejar la temperatura final de la mezcla (Tf).
Paso 4: Resolver la ecuación y obtener la solución
Una vez que hemos aplicado la ley de conservación de la energía y hemos obtenido la ecuación que relaciona los datos y las incógnitas del problema, podemos resolverla para obtener la solución.
Ejemplo:
En el problema anterior, la ecuación que relaciona los datos y las incógnitas es:
m1 * c * (T1 - Tf) = m2 * c * (Tf - T2)
Si despejamos Tf, obtenemos:
Tf = (m1 * c * T1 + m2 * c * T2) / (m1 * c + m2 * c)
Sustituyendo los valores numéricos, obtenemos:
Tf = (500 g * 1 cal/g·°C * 20°C + 300 g * 1 cal/g·°C * 40°C) / (500 g * 1 cal/g·°C + 300 g * 1 cal/g·°C) = 27,6°C
Por lo tanto, la temperatura final de la mezcla será de 27,6°C.
Conclusión
La resolución de problemas de calorimetría puede resultar sencilla si seguimos un esquema que nos ayude a organizar la información y a aplicar los conceptos fundamentales. En este caso, hemos visto que es importante identificar los datos y las incógnitas del problema, aplicar la ley de conservación de la energía y resolver la ecuación resultante para obtener la solución.
Preguntas frecuentes
1. ¿Qué es la capacidad calorífica?
La capacidad calorífica es una propiedad de los cuerpos que indica la cantidad de calor que se necesita para aumentar su temperatura en un grado Celsius. Se expresa en cal/g·°C.
2. ¿Qué es la ley de conservación de la energía?
La ley de conservación de la energía establece que la energía no se crea ni se destruye, sino que se transforma de una forma a otra. En el caso de las transferencias de calor, esto significa que la cantidad de calor que pierde un cuerpo es igual a la cantidad de calor que gana el otro cuerpo.
3. ¿Cómo se calcula la cantidad de calor que se transfiere entre dos cuerpos?
La cantidad de calor que se transfiere entre dos cuerpos se calcula con la fórmula Q = m * c * ΔT, donde m es la masa del cuerpo, c es la capacidad calorífica del material y ΔT es el cambio de temperatura que experimenta el cuerpo.
4. ¿Por qué es importante aplicar la ley de conservación de la energía en la resolución de problemas de calorimetría?
Es importante aplicar la ley de conservación de la energía porque establece una relación entre la cantidad de calor que pierde un cuerpo y la cantidad de calor que gana otro cuerpo. Esta relación nos permite establecer una ecuación que relaciona los datos y las incógnitas del problema y que nos permite resolver el problema de manera sistemática.
5. ¿Qué otros conceptos están relacionados con la calorimetría?
Otros conceptos relacionados con la calorimetría son la entalpía, la entropía y la energía libre de Gibbs. Estos conceptos se utilizan en la termodinámica para describir los procesos que involucran transferencias de calor y de materia.
Deja una respuesta