Descubre fácilmente el número de electrones en la tabla periódica
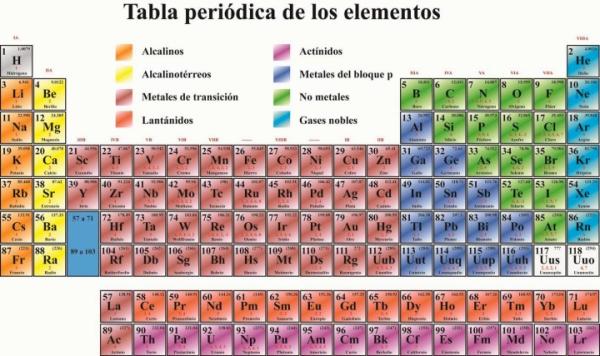
La tabla periódica es una herramienta esencial para cualquier estudiante de química. En ella se encuentran todos los elementos conocidos y su disposición ordenada permite predecir sus propiedades y comportamientos. Una de las informaciones más importantes que se pueden obtener de la tabla periódica es el número de electrones que tiene un átomo de un elemento determinado. En este artículo te enseñaremos cómo descubrirlo fácilmente.
- ¿Qué son los electrones?
- ¿Cómo se determina el número de electrones en un átomo?
- ¿Cómo se lee la tabla periódica para encontrar el número de electrones?
- ¿Cómo se utilizan los grupos de la tabla periódica para predecir el número de electrones?
- ¿Cómo se utiliza la tabla periódica para predecir la carga de un ion?
- Conclusión
- Preguntas frecuentes
- 1. ¿Todos los átomos tienen la misma cantidad de electrones?
- 2. ¿Por qué es importante conocer el número de electrones de un átomo?
- 3. ¿Qué es la capa de valencia?
- 4. ¿Cómo se utilizan los grupos de la tabla periódica para predecir la reactividad de los elementos?
- 5. ¿Cómo se utiliza la tabla periódica para predecir la carga de un ion?
¿Qué son los electrones?
Antes de entrar en materia, es importante saber qué son los electrones. Los electrones son partículas subatómicas con carga negativa que giran alrededor del núcleo del átomo. Son los responsables de las reacciones químicas y de la formación de enlaces entre átomos para crear moléculas.
¿Cómo se determina el número de electrones en un átomo?
El número de electrones en un átomo se determina por su número atómico, que es la cantidad de protones que hay en el núcleo del átomo. Como los átomos son eléctricamente neutros, el número de electrones es igual al número de protones en el núcleo.
Por ejemplo, el hidrógeno tiene un número atómico de 1, lo que significa que tiene un protón en su núcleo y, por lo tanto, un electrón girando alrededor de él. El oxígeno, por otro lado, tiene un número atómico de 8, lo que significa que tiene 8 protones en su núcleo y, por lo tanto, 8 electrones girando a su alrededor.
¿Cómo se lee la tabla periódica para encontrar el número de electrones?
La tabla periódica es una disposición ordenada de los elementos según su número atómico. Los elementos se agrupan en filas y columnas según sus propiedades y su estructura electrónica. La estructura electrónica de un átomo se refiere a la distribución de sus electrones en distintas capas o niveles de energía.
Para encontrar el número de electrones de un átomo en la tabla periódica, debemos fijarnos en su número atómico y su posición en la tabla. El número atómico se encuentra en la parte superior de la caja del elemento y la posición en la tabla nos indica en qué fila se encuentra.
Cada fila de la tabla periódica representa una capa o nivel de energía. La primera fila representa la capa K, la segunda fila representa la capa L, la tercera fila representa la capa M y así sucesivamente.
Por ejemplo, el sodio tiene un número atómico de 11 y se encuentra en la tercera fila de la tabla periódica. Esto significa que tiene 11 electrones y que su estructura electrónica es 2-8-1. Los dos primeros electrones se encuentran en la capa K, los siguientes ocho electrones se encuentran en la capa L y el último electrón se encuentra en la capa M.
¿Cómo se utilizan los grupos de la tabla periódica para predecir el número de electrones?
Los grupos de la tabla periódica también pueden ser útiles para predecir el número de electrones de un átomo. Los grupos son las columnas verticales de la tabla y tienen números del 1 al 18.
Los elementos en el mismo grupo tienen propiedades similares y la misma cantidad de electrones en su capa externa. Esta capa se llama capa de valencia y es la responsable de las propiedades químicas de los elementos.
Por ejemplo, los elementos en el grupo 1 tienen un electrón en su capa de valencia, mientras que los elementos en el grupo 2 tienen dos electrones en su capa de valencia. Los elementos en el grupo 17 tienen siete electrones en su capa de valencia y los elementos en el grupo 18 tienen ocho electrones en su capa de valencia.
¿Cómo se utiliza la tabla periódica para predecir la carga de un ion?
Los electrones también son importantes para predecir la carga de un ion, que es un átomo que ha perdido o ganado electrones para obtener una carga neta positiva o negativa.
Cuando un átomo pierde electrones, se convierte en un ion positivo o catión. Por ejemplo, el sodio pierde un electrón para formar el ion Na+, que tiene una carga neta positiva de 1.
Cuando un átomo gana electrones, se convierte en un ion negativo o anión. Por ejemplo, el cloro gana un electrón para formar el ion Cl-, que tiene una carga neta negativa de 1.
La tabla periódica es útil para predecir la carga de los iones porque los elementos en el mismo grupo tienen la misma cantidad de electrones en su capa de valencia y tienden a ganar o perder electrones para obtener una configuración de valencia completa.
Conclusión
El número de electrones es una información crucial para entender la química de los elementos. La tabla periódica es una herramienta esencial para encontrar esta información y predecir la estructura electrónica de los átomos y los iones. Con un poco de práctica, podrás leer fácilmente la tabla periódica y descubrir el número de electrones de cualquier elemento.
Preguntas frecuentes
1. ¿Todos los átomos tienen la misma cantidad de electrones?
No, la cantidad de electrones en un átomo depende de su número atómico y su posición en la tabla periódica.
2. ¿Por qué es importante conocer el número de electrones de un átomo?
El número de electrones es importante porque determina la estructura electrónica del átomo y su capacidad para formar enlaces y reaccionar químicamente.
3. ¿Qué es la capa de valencia?
La capa de valencia es la capa más externa de un átomo y contiene los electrones de valencia, que son los responsables de las propiedades químicas del elemento.
4. ¿Cómo se utilizan los grupos de la tabla periódica para predecir la reactividad de los elementos?
Los elementos en el mismo grupo tienen propiedades similares porque tienen la misma cantidad de electrones en su capa de valencia. Por lo tanto, se puede predecir la reactividad de un elemento basándose en su posición en el grupo.
5. ¿Cómo se utiliza la tabla periódica para predecir la carga de un ion?
Los elementos tienden a ganar o perder electrones para obtener una configuración de valencia completa. Por lo tanto, se puede predecir la carga de un ion basándose en la cantidad de electrones que ha ganado o perdido.
Deja una respuesta