Cálculo de neutrones, protones y electrones: guía completa
El cálculo de neutrones, protones y electrones es un tema fundamental en la química y la física. Estas partículas subatómicas son los componentes básicos de los átomos y determinan las propiedades de los elementos químicos. En este artículo, te ofreceremos una guía completa para calcular el número de neutrones, protones y electrones de cualquier átomo.
- ¿Qué son los neutrones, protones y electrones?
- ¿Cómo se calcula el número de protones?
- ¿Cómo se calcula el número de electrones?
- ¿Cómo se calcula el número de neutrones?
- Tabla periódica de los elementos
- Conclusión
- Preguntas frecuentes
- 1. ¿Por qué los átomos tienen diferentes números de neutrones?
- 2. ¿Cómo se utilizan los cálculos de neutrones, protones y electrones en la química?
- 3. ¿Qué sucede cuando un átomo pierde o gana electrones?
- 4. ¿Qué es un isótopo?
- 5. ¿Cómo se utiliza la tabla periódica para calcular los neutrones, protones y electrones?
¿Qué son los neutrones, protones y electrones?
Los neutrones, protones y electrones son las tres partículas subatómicas más importantes que componen los átomos. El protón tiene carga positiva, el electrón tiene carga negativa y el neutrón no tiene carga eléctrica. El número de protones en el núcleo de un átomo se conoce como número atómico, y determina el elemento químico al que pertenece el átomo.
¿Cómo se calcula el número de protones?
El número de protones en el núcleo de un átomo es igual al número atómico del elemento. Por ejemplo, el número atómico del hidrógeno es 1, lo que significa que tiene un protón en su núcleo. El número atómico del oxígeno es 8, lo que significa que tiene 8 protones en su núcleo.
¿Cómo se calcula el número de electrones?
El número de electrones en un átomo neutro es igual al número de protones. Sin embargo, los átomos pueden ganar o perder electrones para formar iones con carga positiva o negativa. Por ejemplo, el átomo de sodio tiene 11 electrones en su estado neutro, pero puede perder un electrón para formar un ion con carga positiva (Na+), que tiene 10 electrones.
¿Cómo se calcula el número de neutrones?
El número de neutrones en el núcleo de un átomo puede variar, incluso dentro de un mismo elemento químico. El número de neutrones se puede calcular restando el número atómico del elemento del número de masa del átomo. Por ejemplo, el isótopo más común del carbono es el carbono-12, que tiene 6 protones y 6 neutrones en su núcleo. El carbono-14, por otro lado, tiene 6 protones y 8 neutrones en su núcleo.
Tabla periódica de los elementos
La tabla periódica de los elementos es una herramienta esencial para la química y la física. La tabla periódica enumera todos los elementos químicos conocidos en orden creciente de número atómico. Cada elemento tiene una abreviatura de dos letras, como H para hidrógeno y O para oxígeno, y un número que indica su masa atómica.
Cálculo de neutrones, protones y electrones en los elementos comunes
A continuación, presentamos una lista de algunos elementos comunes y su número de neutrones, protones y electrones:
Hidrógeno
- Número atómico: 1
- Número de protones: 1
- Número de electrones: 1
- Número de neutrones: 0
Oxígeno
- Número atómico: 8
- Número de protones: 8
- Número de electrones: 8
- Número de neutrones: 8
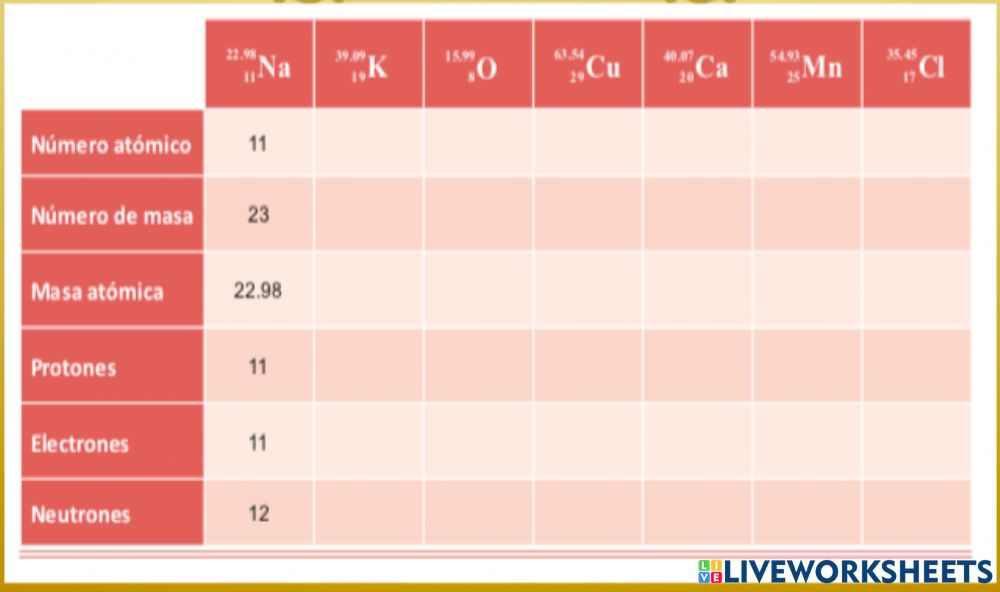
Sodio
- Número atómico: 11
- Número de protones: 11
- Número de electrones: 11
- Número de neutrones: 12
Calcio
- Número atómico: 20
- Número de protones: 20
- Número de electrones: 20
- Número de neutrones: 20
Hierro
- Número atómico: 26
- Número de protones: 26
- Número de electrones: 26
- Número de neutrones: 30
Cálculo de neutrones, protones y electrones en iones
Los iones son átomos que han ganado o perdido electrones para formar una carga eléctrica positiva o negativa. El número de protones no cambia en un ion, pero el número de electrones sí. Por lo tanto, el número de neutrones en un ion sigue siendo el mismo que en el átomo neutro.
Ión sodio (Na+)
- Número de protones: 11
- Número de electrones: 10
- Número de neutrones: 12
Ión cloruro (Cl-)
- Número de protones: 17
- Número de electrones: 18
- Número de neutrones: 18
Conclusión
El cálculo de neutrones, protones y electrones es un aspecto fundamental de la química y la física. Estas partículas subatómicas determinan las propiedades de los elementos químicos y son esenciales para comprender la estructura de la materia. Con la información proporcionada en este artículo, podrás calcular fácilmente el número de neutrones, protones y electrones de cualquier átomo.
Preguntas frecuentes
1. ¿Por qué los átomos tienen diferentes números de neutrones?
Los átomos de un mismo elemento químico pueden tener diferentes números de neutrones, lo que se conoce como isótopos. Los isótopos tienen propiedades químicas similares, pero pueden tener diferentes masas atómicas y ser radiactivos.
2. ¿Cómo se utilizan los cálculos de neutrones, protones y electrones en la química?
Los cálculos de neutrones, protones y electrones se utilizan para determinar la estructura de los átomos y las propiedades de los elementos químicos. Estos cálculos son esenciales para comprender la estructura de la materia y para diseñar nuevas moléculas y materiales.
3. ¿Qué sucede cuando un átomo pierde o gana electrones?
Cuando un átomo pierde electrones, se convierte en un ion con carga positiva. Cuando un átomo gana electrones, se convierte en un ion con carga negativa. Los iones pueden formar enlaces químicos con otros iones o átomos para formar moléculas y compuestos.
4. ¿Qué es un isótopo?
Un isótopo es un átomo de un elemento químico que tiene el mismo número de protones pero un número diferente de neutrones en su núcleo. Los isótopos pueden tener diferentes masas atómicas y propiedades físicas y químicas.
5. ¿Cómo se utiliza la tabla periódica para calcular los neutrones, protones y electrones?
La tabla periódica enumera todos los elementos químicos conocidos en orden creciente de número atómico. El número atómico indica el número de protones en el núcleo de un átomo,
Deja una respuesta