Configuración electrónica: aprende a hacerla fácilmente
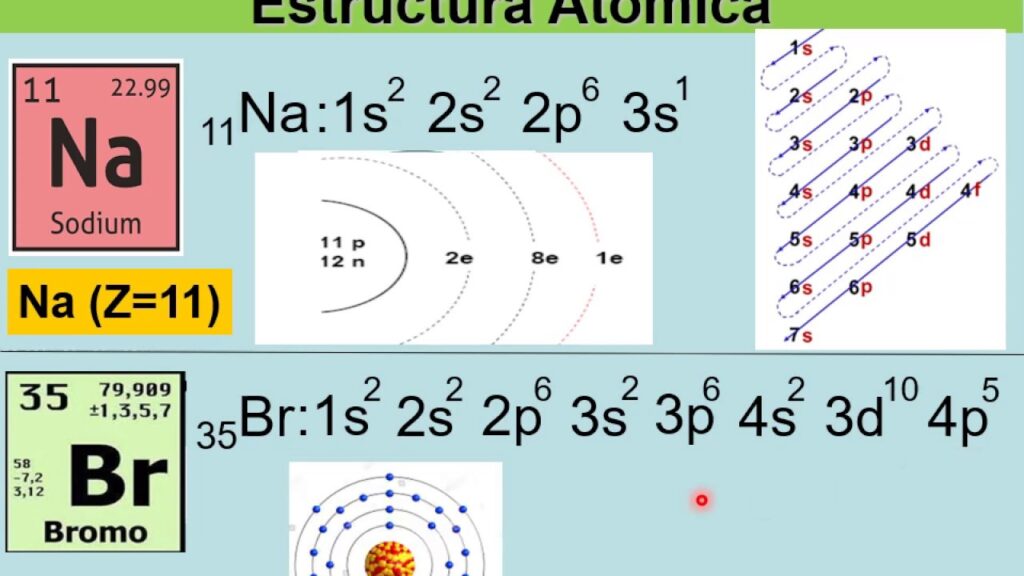
La configuración electrónica es la distribución de electrones en los diferentes niveles y subniveles de energía de un átomo. Esta distribución puede parecer complicada a primera vista, pero en realidad es bastante sencilla si se entienden algunos conceptos básicos. En este artículo, te explicaremos cómo hacer la configuración electrónica de manera fácil y comprensible.
- ¿Qué son los niveles y subniveles de energía?
- Regla de Aufbau
- Principio de exclusión de Pauli
- Configuración electrónica abreviada
- Configuración electrónica de los elementos
- Conclusión
- Preguntas frecuentes
- 1. ¿Por qué es importante conocer la configuración electrónica?
- 2. ¿Cómo se determina la configuración electrónica de un elemento?
- 3. ¿Qué es la configuración electrónica abreviada?
- 4. ¿Cómo se representa un electrón en un diagrama de configuración electrónica?
- 5. ¿Cómo afecta la configuración electrónica a las propiedades de un elemento?
¿Qué son los niveles y subniveles de energía?
Antes de entrar en la configuración electrónica, es importante entender qué son los niveles y subniveles de energía. Los niveles de energía son capas que rodean al núcleo del átomo y están numerados del 1 al 7 (K, L, M, N, O, P, Q). Cada nivel puede contener un número máximo de electrones y a medida que se avanza en los niveles, la energía de los electrones aumenta.
Los subniveles de energía se dividen en s, p, d y f. El subnivel s tiene forma esférica y puede contener hasta 2 electrones, el subnivel p tiene forma de lágrima y puede contener hasta 6 electrones, el subnivel d tiene forma de doble lágrima y puede contener hasta 10 electrones, y el subnivel f tiene forma compleja y puede contener hasta 14 electrones.
Regla de Aufbau
La regla de Aufbau es un principio que establece que los electrones llenan los niveles y subniveles de energía en orden ascendente de energía. Es decir, primero se llenan los subniveles de menor energía antes de pasar a los subniveles de mayor energía. Por ejemplo, el subnivel 4s se llena antes que el subnivel 3d.
Principio de exclusión de Pauli
El principio de exclusión de Pauli establece que dos electrones en un átomo no pueden tener los mismos cuatro números cuánticos. Estos números cuánticos son el número cuántico principal (n), el número cuántico secundario (l), el número cuántico magnético (m) y el número cuántico de espín (s).
Configuración electrónica abreviada
La configuración electrónica abreviada es una forma más sencilla de escribir la configuración electrónica. En lugar de escribir todos los electrones, solo se escriben los electrones de los niveles y subniveles de energía más externos. Por ejemplo, la configuración electrónica abreviada del calcio (Ca) es [Ar] 4s2, lo que significa que los electrones de los niveles anteriores (K, L y M) se representan por el elemento argón (Ar) y los dos electrones restantes se encuentran en el subnivel 4s.
Configuración electrónica de los elementos
A continuación, se muestra la configuración electrónica de algunos elementos comunes:
- Hidrógeno (H): 1s1
- Helio (He): 1s2
- Carbono (C): [He] 2s2 2p2
- Nitrógeno (N): [He] 2s2 2p3
- Oxígeno (O): [He] 2s2 2p4
- Hierro (Fe): [Ar] 3d6 4s2
- Oro (Au): [Xe] 4f14 5d10 6s1
Conclusión
La configuración electrónica puede parecer complicada, pero es fácil de entender si se conocen los conceptos básicos. Recuerda que los electrones llenan los niveles y subniveles de energía en orden ascendente, y que dos electrones no pueden tener los mismos cuatro números cuánticos. La configuración electrónica abreviada es una forma sencilla de escribir la configuración electrónica de un elemento.
Preguntas frecuentes
1. ¿Por qué es importante conocer la configuración electrónica?
La configuración electrónica es importante porque determina las propiedades químicas y físicas de un elemento. Por ejemplo, la reactividad química de un elemento depende de la cantidad de electrones que tiene en su capa externa.
2. ¿Cómo se determina la configuración electrónica de un elemento?
La configuración electrónica de un elemento se determina por la posición del elemento en la tabla periódica y siguiendo la regla de Aufbau y el principio de exclusión de Pauli.
3. ¿Qué es la configuración electrónica abreviada?
La configuración electrónica abreviada es una forma más sencilla de escribir la configuración electrónica. En lugar de escribir todos los electrones, solo se escriben los electrones de los niveles y subniveles de energía más externos.
4. ¿Cómo se representa un electrón en un diagrama de configuración electrónica?
Un electrón se representa con una flecha hacia arriba o hacia abajo para indicar su espín. Los electrones con espín hacia arriba se representan con una flecha hacia arriba y los electrones con espín hacia abajo se representan con una flecha hacia abajo.
5. ¿Cómo afecta la configuración electrónica a las propiedades de un elemento?
La configuración electrónica afecta las propiedades de un elemento al determinar su reactividad química, su capacidad para formar enlaces químicos y su capacidad para conducir electricidad y calor, entre otras propiedades físicas y químicas.
Deja una respuesta