Descubre la masa atómica de los elementos: concepto y aplicaciones
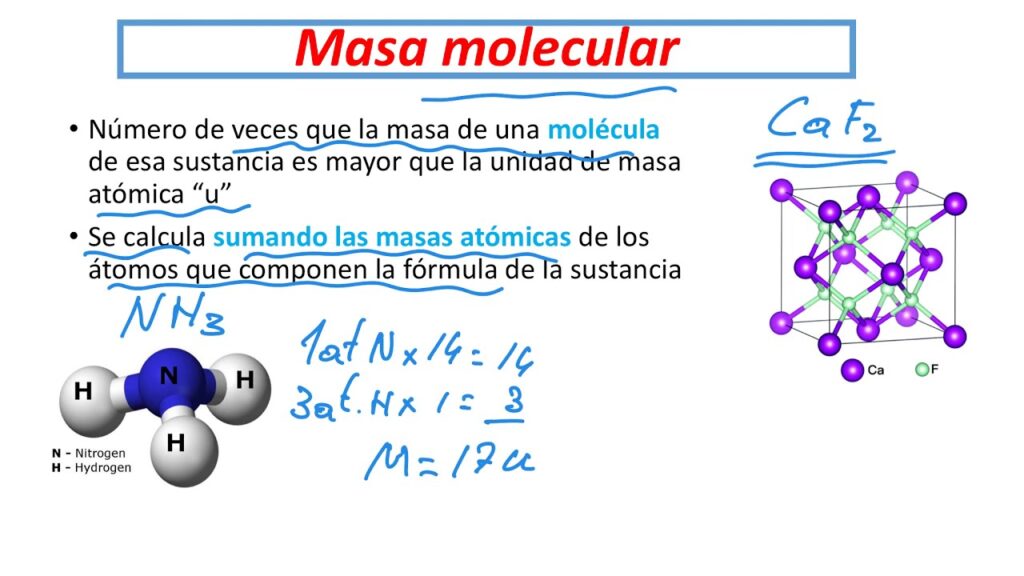
La masa atómica es uno de los conceptos fundamentales en la química, ya que nos permite conocer la masa de los átomos de los diferentes elementos que forman la materia. En este artículo, te explicaremos qué es la masa atómica, cómo se calcula y cuáles son algunas de sus aplicaciones.
¿Qué es la masa atómica?
La masa atómica es la masa de un átomo de un elemento determinado, expresada en unidades de masa atómica (uma). Esta unidad de medida se define como la doceava parte de la masa de un átomo de carbono-12.
Es importante destacar que la masa atómica no es lo mismo que el número atómico, que es el número de protones que tiene un átomo en su núcleo. La masa atómica incluye la masa de los protones y neutrones en el núcleo, así como la masa de los electrones que giran alrededor del núcleo.
¿Cómo se calcula la masa atómica?
La masa atómica se calcula sumando la masa de los protones y neutrones en el núcleo de un átomo. Como la masa de los electrones es mucho menor, se considera despreciable en este cálculo.
Es importante destacar que la masa atómica no es un número entero, ya que la mayoría de los elementos tienen diferentes isótopos, que son átomos del mismo elemento con diferente número de neutrones. Por lo tanto, la masa atómica que se utiliza en la tabla periódica es un promedio ponderado de las masas de los isótopos de cada elemento, teniendo en cuenta su abundancia relativa.
¿Para qué se utiliza la masa atómica?
La masa atómica tiene numerosas aplicaciones en la química y otras áreas de la ciencia. Algunas de las más importantes son:
1. Determinar la cantidad de átomos en una muestra
La masa atómica se utiliza para convertir la masa de una muestra de un elemento en el número de átomos presentes en ella. Por ejemplo, si tenemos una muestra de 10 gramos de carbono con una masa atómica de 12,01 uma, podemos calcular que hay aproximadamente 8,32 x 10^23 átomos de carbono en esa muestra.
2. Calcular la cantidad de sustancia en una muestra
La masa atómica también se utiliza para calcular la cantidad de sustancia en una muestra de un compuesto químico. Por ejemplo, si tenemos una muestra de 10 gramos de dióxido de carbono (CO2), podemos calcular que hay aproximadamente 0,208 moles de CO2 en esa muestra, utilizando la masa atómica del carbono y del oxígeno.
3. Identificar elementos desconocidos
La masa atómica se utiliza para identificar elementos desconocidos a través de la espectrometría de masas. En esta técnica, se mide la masa de los iones producidos por la fragmentación de una muestra en un espectrómetro de masas. La comparación de las masas de los iones con la masa atómica conocida de los elementos permite identificar los elementos presentes en la muestra.
4. Calcular la energía de enlace
La masa atómica también se utiliza para calcular la energía de enlace en los compuestos químicos. La energía de enlace es la energía necesaria para romper los enlaces químicos en un compuesto y separar los átomos. La masa atómica se utiliza para calcular la masa total de los átomos en un compuesto, lo que a su vez se utiliza para calcular la energía de enlace.
Tabla periódica y masa atómica
La tabla periódica es una herramienta fundamental para la química y la física, que organiza los elementos en función de su estructura atómica y sus propiedades químicas. En la tabla periódica, cada elemento se presenta con su símbolo y su masa atómica.
Es importante destacar que la masa atómica que se presenta en la tabla periódica es un promedio ponderado de las masas de los isótopos de cada elemento, teniendo en cuenta su abundancia relativa. Por ejemplo, el carbono tiene dos isótopos estables: el carbono-12, que tiene una abundancia del 98,9%, y el carbono-13, que tiene una abundancia del 1,1%. Por lo tanto, la masa atómica del carbono que se presenta en la tabla periódica es de 12,01 uma, que es el promedio ponderado de las masas de los isótopos.
Conclusión
La masa atómica es un concepto fundamental en la química, que nos permite conocer la masa de los átomos de los diferentes elementos que forman la materia. Se calcula sumando la masa de los protones y neutrones en el núcleo de un átomo, y se utiliza en numerosas aplicaciones en la química y otras áreas de la ciencia. La tabla periódica es una herramienta fundamental para la química y la física, que organiza los elementos en función de su estructura atómica y sus propiedades químicas, y presenta la masa atómica de cada elemento.
Preguntas frecuentes
1. ¿Por qué la masa atómica no es un número entero?
La masa atómica no es un número entero porque la mayoría de los elementos tienen diferentes isótopos, que son átomos del mismo elemento con diferente número de neutrones. Por lo tanto, la masa atómica que se utiliza en la tabla periódica es un promedio ponderado de las masas de los isótopos de cada elemento, teniendo en cuenta su abundancia relativa.
2. ¿Cómo se utiliza la masa atómica para determinar la cantidad de átomos en una muestra?
La masa atómica se utiliza para convertir la masa de una muestra de un elemento en el número de átomos presentes en ella. Por ejemplo, si tenemos una muestra de 10 gramos de carbono con una masa atómica de 12,01 uma, podemos calcular que hay aproximadamente 8,32 x 10^23 átomos de carbono en esa muestra.
3. ¿Qué es la espectrometría de masas?
La espectrometría de masas es una técnica analítica que se utiliza para identificar los componentes de una muestra mediante la medición de la masa de los iones que se producen por la fragmentación de la muestra en un espectrómetro de masas.
4. ¿Qué es la energía de enlace?
La energía de enlace es la energía necesaria para romper los enlaces químicos en un compuesto y separar los átomos. La masa atómica se utiliza para calcular la masa total de los átomos en un compuesto, lo que a su vez se utiliza para calcular la energía de enlace.
5. ¿Por qué la tabla periódica es importante para la química y la física?
La tabla periódica es importante para la química y la física porque organiza los elementos en función de su estructura atómica y
Deja una respuesta