Descubre el modelo atómico de Rutherford: estructura y funcionamiento
Si te interesa la química o la física, seguramente habrás escuchado hablar del modelo atómico de Rutherford. Este modelo fue propuesto por el físico neozelandés Ernest Rutherford en 1911 y supuso un gran avance en la comprensión de la estructura del átomo. En este artículo, vamos a explicar en qué consiste el modelo atómico de Rutherford, cómo funciona y cuál fue su importancia en la historia de la ciencia.
- ¿En qué consiste el modelo atómico de Rutherford?
- ¿Cómo funciona el modelo atómico de Rutherford?
- ¿Cuál fue la importancia del modelo atómico de Rutherford?
- Preguntas frecuentes
- 1. ¿Cómo se comparan los modelos atómicos de Rutherford y Bohr?
- 2. ¿Es el modelo atómico de Rutherford todavía válido?
- 3. ¿Cómo afectó el modelo atómico de Rutherford al desarrollo de la bomba atómica?
- 4. ¿Qué relación tiene el modelo atómico de Rutherford con la radioactividad?
- 5. ¿Por qué es importante conocer la estructura del átomo?
¿En qué consiste el modelo atómico de Rutherford?
Antes de que Rutherford propusiera su modelo atómico, se creía que el átomo era una estructura homogénea, en la que los electrones estaban distribuidos uniformemente alrededor de un núcleo. Sin embargo, Rutherford descubrió que la realidad era muy diferente. Realizó un experimento en el que bombardeó una lámina de oro con partículas alfa (núcleos de helio) y observó cómo se comportaban estas partículas al interactuar con los átomos de la lámina.
Lo que Rutherford observó fue que la mayoría de las partículas alfa pasaban a través de la lámina sin desviarse, pero algunas eran desviadas en ángulos muy grandes. Esto indicaba que la lámina de oro contenía una concentración muy alta de carga positiva en un espacio muy reducido, lo que hacía que algunas partículas alfa fueran desviadas por la repulsión electrostática.
A partir de este experimento, Rutherford propuso que el átomo estaba compuesto por un núcleo central muy denso y cargado positivamente, alrededor del cual giraban los electrones. Esta idea revolucionaria permitió explicar muchas de las propiedades del átomo que se conocían en ese momento, como la emisión de rayos X o la naturaleza eléctrica de la materia.
¿Cómo funciona el modelo atómico de Rutherford?
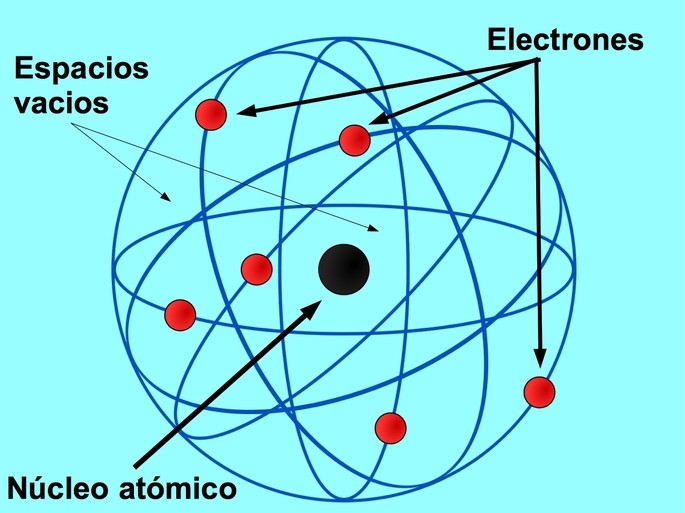
El modelo atómico de Rutherford describe el átomo como un sistema formado por un núcleo central, que contiene protones y neutrones, rodeado por los electrones, que giran en órbitas alrededor del núcleo. El núcleo es muy pequeño en comparación con el tamaño del átomo, pero contiene la mayor parte de la masa del mismo.
Los electrones están distribuidos en diferentes niveles de energía, que se corresponden con diferentes órbitas alrededor del núcleo. Cada nivel de energía puede contener un número máximo de electrones, y los electrones pueden saltar de una órbita a otra si absorben o emiten energía.
La carga eléctrica del núcleo es igual a la suma de las cargas positivas de los protones que contiene. Esta carga positiva atrae a los electrones, que tienen carga negativa, y mantiene al átomo unido. Sin embargo, la repulsión entre los electrones que se encuentran en la misma órbita hace que el átomo tenga una estructura estable y equilibrada.
¿Cuál fue la importancia del modelo atómico de Rutherford?
El modelo atómico de Rutherford supuso un gran avance en la comprensión de la estructura del átomo y permitió explicar muchos de los fenómenos que se conocían en ese momento, como la emisión de rayos X o la naturaleza eléctrica de la materia. Además, este modelo sentó las bases para el desarrollo de otros modelos atómicos más complejos, como el modelo cuántico actual.
El modelo atómico de Rutherford también tuvo implicaciones importantes en otras áreas de la ciencia, como la química y la física nuclear. Por ejemplo, permitió entender cómo se producen las reacciones químicas y cómo se generan las radiaciones ionizantes.
Preguntas frecuentes
1. ¿Cómo se comparan los modelos atómicos de Rutherford y Bohr?
El modelo atómico de Bohr, propuesto en 1913, fue una mejora del modelo de Rutherford. En el modelo de Bohr, los electrones se encuentran en órbitas circulares alrededor del núcleo, pero solo pueden ocupar ciertos niveles de energía bien definidos. Además, los electrones pueden saltar de una órbita a otra si absorben o emiten energía.
2. ¿Es el modelo atómico de Rutherford todavía válido?
El modelo atómico de Rutherford fue una aproximación útil para entender la estructura del átomo en su momento, pero hoy en día se sabe que la realidad es mucho más compleja. El modelo cuántico actual describe el átomo como una nube de probabilidad de electrones, en lugar de órbitas bien definidas.
3. ¿Cómo afectó el modelo atómico de Rutherford al desarrollo de la bomba atómica?
El modelo atómico de Rutherford permitió entender cómo se producen las reacciones nucleares y cómo se liberan grandes cantidades de energía. Estos conocimientos fueron esenciales para el desarrollo de la bomba atómica durante la Segunda Guerra Mundial.
4. ¿Qué relación tiene el modelo atómico de Rutherford con la radioactividad?
El modelo atómico de Rutherford permitió entender cómo se produce la radiactividad y cómo se desintegran los átomos. A partir de este modelo, se pudo explicar la emisión de partículas alfa y beta, así como la naturaleza inestable de algunos núcleos atómicos.
5. ¿Por qué es importante conocer la estructura del átomo?
La estructura del átomo es fundamental para entender muchas de las propiedades de la materia y para desarrollar tecnologías como la energía nuclear o la electrónica. Además, el conocimiento de la estructura del átomo ha permitido a los científicos desarrollar nuevas teorías y modelos para explicar fenómenos aún más complejos, como la estructura de las moléculas o la naturaleza de la materia oscura.
Deja una respuesta