¿Átomo o molécula? Descubre cuál es más pequeño
Cuando hablamos de las cosas más pequeñas en el mundo, es común que se nos vengan a la mente los términos átomo y molécula. Ambos son fundamentales en la química y la física, pero ¿cuál es más pequeño? En este artículo te lo explicamos.
- ¿Qué es un átomo?
- ¿Qué es una molécula?
- ¿Cuál es más pequeño: átomo o molécula?
- ¿Cómo se miden los átomos y las moléculas?
- ¿Por qué es importante conocer el tamaño de los átomos y las moléculas?
- Conclusión
- Preguntas frecuentes
- ¿Por qué los átomos son más pequeños que las moléculas?
- ¿Cómo se miden los átomos y las moléculas?
- ¿Por qué es importante conocer el tamaño de los átomos y las moléculas?
- ¿Qué es un enlace químico?
- ¿Cómo influye el tamaño de los átomos y las moléculas en las propiedades químicas de los elementos y compuestos?
¿Qué es un átomo?
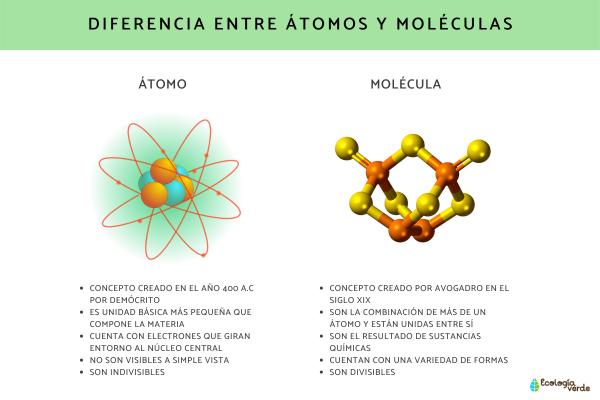
Un átomo es la unidad básica de la materia, es decir, la estructura más pequeña que mantiene las propiedades químicas de un elemento. Está compuesto por un núcleo central, donde se encuentran los protones y neutrones, y por electrones que giran alrededor del núcleo.
¿Qué es una molécula?
Una molécula, por otro lado, es una estructura formada por dos o más átomos unidos mediante enlaces químicos. Las moléculas pueden ser de elementos distintos o iguales, y pueden ser simples o complejas, dependiendo de la cantidad de átomos que las componen.
¿Cuál es más pequeño: átomo o molécula?
Ahora bien, llegamos al punto crucial de esta discusión: ¿cuál es más pequeño, el átomo o la molécula? La respuesta es sencilla: el átomo es más pequeño que la molécula.
Esto se debe a que la molécula está compuesta por dos o más átomos unidos mediante enlaces químicos, lo que implica que su tamaño es mayor que el de los átomos que la componen. Por ejemplo, una molécula de agua está compuesta por dos átomos de hidrógeno y uno de oxígeno, por lo que su tamaño es mayor que el de un solo átomo de hidrógeno o de oxígeno.
¿Cómo se miden los átomos y las moléculas?
La medida más común para expresar el tamaño de los átomos y las moléculas es el ángstrom, que equivale a 0.1 nanómetros o 1x10^-10 metros. Aunque estos tamaños son extremadamente pequeños, son fundamentales en la comprensión de la química y la física.
¿Por qué es importante conocer el tamaño de los átomos y las moléculas?
Conocer el tamaño de los átomos y las moléculas es importante en muchos campos de la ciencia, como la química, la física, la biología y la medicina. Por ejemplo, en la química, el tamaño de los átomos y las moléculas influye en las propiedades químicas de los elementos y compuestos, como su reactividad, solubilidad y conductividad.
En la medicina, el tamaño de los átomos y las moléculas es fundamental en la comprensión de cómo funcionan los medicamentos y cómo interactúan con el cuerpo humano. Además, el conocimiento del tamaño de los átomos y las moléculas es fundamental en la síntesis de nuevos compuestos y materiales.
Conclusión
Aunque tanto el átomo como la molécula son fundamentales en la química y la física, el átomo es más pequeño que la molécula. Conocer el tamaño de los átomos y las moléculas es importante en muchos campos de la ciencia, y es fundamental en la comprensión de cómo funcionan los elementos y compuestos que nos rodean.
Preguntas frecuentes
¿Por qué los átomos son más pequeños que las moléculas?
Los átomos son más pequeños que las moléculas porque la molécula está compuesta por dos o más átomos unidos mediante enlaces químicos, lo que implica que su tamaño es mayor que el de los átomos que la componen.
¿Cómo se miden los átomos y las moléculas?
La medida más común para expresar el tamaño de los átomos y las moléculas es el ángstrom, que equivale a 0.1 nanómetros o 1x10^-10 metros.
¿Por qué es importante conocer el tamaño de los átomos y las moléculas?
Conocer el tamaño de los átomos y las moléculas es importante en muchos campos de la ciencia, como la química, la física, la biología y la medicina. Es fundamental en la comprensión de cómo funcionan los elementos y compuestos que nos rodean.
¿Qué es un enlace químico?
Un enlace químico es una fuerza que mantiene unidos a dos o más átomos para formar una molécula. Los enlaces químicos pueden ser iónicos, covalentes o metálicos, dependiendo de la forma en que se comparten o transfieren los electrones.
¿Cómo influye el tamaño de los átomos y las moléculas en las propiedades químicas de los elementos y compuestos?
El tamaño de los átomos y las moléculas influye en las propiedades químicas de los elementos y compuestos, como su reactividad, solubilidad y conductividad. Por ejemplo, los átomos más grandes tienden a tener una mayor reactividad y una menor solubilidad que los átomos más pequeños.
Deja una respuesta