Distribución electrónica: cómo se organizan los electrones en el átomo
En el mundo de la química, la distribución electrónica es un tema fundamental para entender cómo se organizan los electrones en el átomo. Los electrones son partículas subatómicas que giran alrededor del núcleo del átomo y son responsables de muchas de las propiedades químicas y físicas de los elementos. En este artículo, vamos a explorar cómo se organizan los electrones en el átomo y cómo esto afecta su comportamiento químico.
- ¿Qué es la distribución electrónica?
- ¿Cómo se organizan los electrones en el átomo?
- ¿Cómo afecta la distribución electrónica el comportamiento químico?
- ¿Cómo se puede determinar la distribución electrónica de un átomo?
- ¿Cómo se puede representar la distribución electrónica de un átomo?
- Conclusión
- Preguntas frecuentes
- 1. ¿Qué es la distribución electrónica?
- 2. ¿Cómo se organizan los electrones en el átomo?
- 3. ¿Cómo afecta la distribución electrónica el comportamiento químico?
- 4. ¿Cómo se puede determinar la distribución electrónica de un átomo?
- 5. ¿Cómo se puede representar la distribución electrónica de un átomo?
¿Qué es la distribución electrónica?
La distribución electrónica es el patrón de cómo están organizados los electrones en el átomo. Los electrones se organizan en capas, también conocidas como niveles energéticos, que están numeradas del uno al siete. Estos niveles energéticos están divididos en subniveles, que se designan por las letras s, p, d y f. El número de electrones que un átomo tiene en cada nivel energético y subnivel determina sus propiedades químicas.
¿Cómo se organizan los electrones en el átomo?
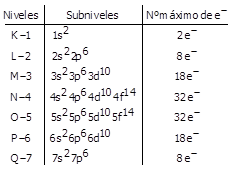
Los electrones se organizan en capas, comenzando por la capa más cercana al núcleo. La capa más cercana al núcleo se llama la capa K, seguida por la capa L, la capa M, la capa N, la capa O, la capa P y la capa Q. Cada capa puede contener un número máximo de electrones, que se calcula utilizando la fórmula 2n². Por ejemplo, la capa K puede contener hasta 2 electrones, la capa L puede contener hasta 8 electrones, y la capa M puede contener hasta 18 electrones.
Los subniveles se organizan dentro de las capas. El subnivel s es el más cercano al núcleo y puede contener hasta 2 electrones. El subnivel p puede contener hasta 6 electrones, el subnivel d puede contener hasta 10 electrones y el subnivel f puede contener hasta 14 electrones.
Ejemplo:
El hidrógeno tiene un electrón en su capa más externa, la capa K. Su configuración electrónica es 1s¹. El helio tiene dos electrones en su capa K y su configuración electrónica es 1s². El sodio tiene una configuración electrónica de 1s²2s²2p⁶3s¹, lo que significa que tiene dos electrones en su capa K, ocho electrones en su capa L y un electrón en su subnivel 3s.
¿Cómo afecta la distribución electrónica el comportamiento químico?
La distribución electrónica determina las propiedades químicas de un átomo. Los átomos con la misma configuración electrónica en su capa más externa tienen propiedades químicas similares. Estos átomos se encuentran en la misma columna de la tabla periódica y se denominan elementos del mismo grupo.
Por ejemplo, los elementos del grupo 1 (litio, sodio, potasio, rubidio, cesio y francio) tienen un electrón en su capa más externa y son muy reactivos. Estos elementos tienen una tendencia a perder su electrón externo para formar iones con una carga positiva.
Los elementos del grupo 17 (flúor, cloro, bromo, yodo y astato) tienen siete electrones en su capa más externa y son muy reactivos. Estos elementos tienen una tendencia a ganar un electrón para formar iones con una carga negativa.
¿Cómo se puede determinar la distribución electrónica de un átomo?
La distribución electrónica de un átomo se puede determinar utilizando la tabla periódica. Cada elemento químico está representado por un símbolo y un número atómico, que indica el número de protones en el núcleo del átomo. La distribución electrónica se puede determinar utilizando la regla de configuración electrónica de Aufbau, que establece que los electrones se llenan en el orden de menor a mayor energía.
¿Cómo se puede representar la distribución electrónica de un átomo?
La distribución electrónica se puede representar utilizando la notación de configuración electrónica abreviada. En esta notación, el símbolo del elemento se escribe primero, seguido de la configuración electrónica abreviada. Por ejemplo, la configuración electrónica abreviada del sodio es [Ne]3s¹.
Conclusión
La distribución electrónica es un tema fundamental en la química que nos permite entender cómo se organizan los electrones en el átomo y cómo esto afecta su comportamiento químico. Los electrones se organizan en capas y subniveles, y la distribución electrónica determina las propiedades químicas de un átomo. La distribución electrónica se puede determinar utilizando la tabla periódica y se puede representar utilizando la notación de configuración electrónica abreviada.
Preguntas frecuentes
1. ¿Qué es la distribución electrónica?
La distribución electrónica es el patrón de cómo están organizados los electrones en el átomo.
2. ¿Cómo se organizan los electrones en el átomo?
Los electrones se organizan en capas y subniveles dentro del átomo.
3. ¿Cómo afecta la distribución electrónica el comportamiento químico?
La distribución electrónica determina las propiedades químicas de un átomo y puede afectar su capacidad para formar enlaces químicos.
4. ¿Cómo se puede determinar la distribución electrónica de un átomo?
La distribución electrónica de un átomo se puede determinar utilizando la tabla periódica y la regla de configuración electrónica de Aufbau.
5. ¿Cómo se puede representar la distribución electrónica de un átomo?
La distribución electrónica se puede representar utilizando la notación de configuración electrónica abreviada, en la que el símbolo del elemento se escribe primero, seguido de la configuración electrónica abreviada.
Deja una respuesta