Descubre las partículas esenciales del átomo en este breve resumen
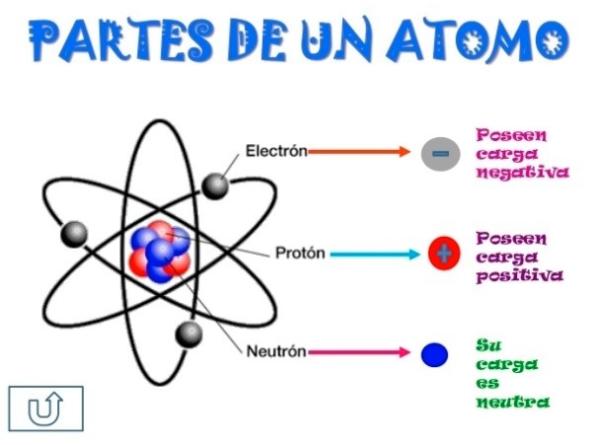
El átomo es la unidad básica de la materia, y se compone de varias partículas esenciales. En este artículo, te explicaremos cuáles son estas partículas y cuál es su función en la estructura del átomo.
El núcleo
El núcleo es el centro del átomo y está formado por protones y neutrones. Los protones tienen carga positiva, mientras que los neutrones no tienen carga. Juntos, los protones y los neutrones forman la mayor parte de la masa del átomo.
Los electrones
Los electrones son partículas que orbitan alrededor del núcleo. Tienen carga negativa y son mucho más pequeños que los protones y los neutrones. Los electrones son los responsables de las propiedades químicas del átomo, ya que su distribución en las capas electrónicas determina cómo se comporta el átomo en las reacciones químicas.
La carga eléctrica
La carga eléctrica es una propiedad esencial de las partículas del átomo. Los protones tienen carga positiva, los electrones tienen carga negativa y los neutrones no tienen carga. La carga eléctrica de un átomo se mide en unidades llamadas electronvoltios (eV).
El número atómico
El número atómico de un átomo es la cantidad de protones que hay en su núcleo. Este número determina el tipo de elemento químico al que pertenece el átomo. Por ejemplo, todos los átomos de hidrógeno tienen un número atómico de 1, mientras que todos los átomos de oxígeno tienen un número atómico de 8.
El peso atómico
El peso atómico de un átomo es la suma de la masa de sus protones y neutrones. Se expresa en unidades de masa atómica (uma). Para calcular el peso atómico de un elemento químico, se multiplica el número de átomos de cada isótopo por su peso atómico y se divide por el número total de átomos del elemento.
Los isótopos
Los isótopos son átomos de un mismo elemento que tienen el mismo número de protones, pero un número diferente de neutrones. Esto significa que tienen el mismo número atómico, pero un peso atómico diferente. Los isótopos pueden ser estables o inestables y algunos de ellos son radiactivos.
La configuración electrónica
La configuración electrónica es la distribución de los electrones en las capas electrónicas del átomo. Esta distribución determina las propiedades químicas del átomo y su capacidad para formar enlaces químicos con otros átomos. La configuración electrónica se representa mediante una serie de números y letras que indican el número de electrones en cada capa electrónica.
Los enlaces químicos
Los enlaces químicos son las fuerzas que mantienen unidos los átomos en una molécula. Pueden ser iónicos, covalentes o metálicos, dependiendo de la forma en que se comparten o transfieren los electrones entre los átomos. Los enlaces químicos son esenciales para la formación de compuestos químicos y para la vida en general.
La tabla periódica
La tabla periódica es una herramienta esencial para la química y la física. En ella se organizan todos los elementos químicos en función de su número atómico y su configuración electrónica. La tabla periódica permite predecir las propiedades químicas de los elementos y facilita la identificación de nuevos compuestos y elementos químicos.
Conclusión
El átomo está formado por tres partículas esenciales: protones, neutrones y electrones. Cada una de estas partículas tiene una función específica en la estructura y las propiedades del átomo. Comprender las propiedades del átomo es esencial para entender la química y la física, y para el desarrollo de nuevas tecnologías y materiales.
Preguntas frecuentes
¿Cuál es la diferencia entre un átomo y una molécula?
Un átomo es la unidad básica de la materia, mientras que una molécula está formada por dos o más átomos unidos por enlaces químicos. En otras palabras, los átomos son los bloques de construcción de las moléculas.
¿Por qué los electrones son importantes en la química?
Los electrones son importantes en la química porque su distribución en las capas electrónicas determina las propiedades químicas del átomo. La forma en que los electrones se comparten o transfieren entre los átomos es lo que determina la formación de enlaces químicos y la creación de compuestos químicos.
¿Qué es un isótopo radiactivo?
Un isótopo radiactivo es un átomo que tiene un número diferente de neutrones en su núcleo y que es inestable. Como resultado, emite radiación en forma de partículas alfa, beta o gamma. Los isótopos radiactivos se utilizan en medicina, investigación y energía nuclear.
¿Cómo se relacionan el número atómico y el peso atómico?
El número atómico y el peso atómico están relacionados porque el número atómico determina la cantidad de protones en el núcleo del átomo, mientras que el peso atómico es la suma de la masa de los protones y los neutrones. En general, el peso atómico aumenta a medida que aumenta el número atómico.
¿Por qué es importante la tabla periódica?
La tabla periódica es importante porque permite organizar los elementos químicos en función de sus propiedades y su estructura atómica. Esto facilita la identificación de nuevos elementos y compuestos químicos, y permite predecir las propiedades de los elementos y sus compuestos. La tabla periódica también es esencial para la educación y la investigación en química y física.
Deja una respuesta