La ley de conservación de la materia: la clave de la química
La química es una ciencia que estudia la composición, estructura, propiedades y transformaciones de la materia. Y una de las leyes fundamentales en esta disciplina es la ley de conservación de la materia.
Esta ley establece que en una reacción química, la cantidad total de materia antes y después de la reacción es la misma. En otras palabras, la materia no se crea ni se destruye, solo se transforma.
Esta idea puede resultar un tanto abstracta, pero una analogía sencilla puede ayudarnos a entenderla mejor. Imagina que tienes una pizza y la cortas en cuatro pedazos. A simple vista, parece que la cantidad de pizza ha aumentado, pero en realidad sigue siendo la misma cantidad de materia. Lo único que ha cambiado es la forma en que está distribuida.
Esta ley es esencial en la química ya que nos permite predecir qué sucederá en una reacción química y cómo se comportarán las sustancias involucradas. En otras palabras, nos ayuda a entender cómo se transforma la materia y cómo podemos controlar esas transformaciones.
Para comprender mejor la ley de conservación de la materia, es importante entender algunos conceptos básicos de la química, como los átomos y las moléculas. Los átomos son las unidades básicas de la materia, y las moléculas están formadas por la unión de dos o más átomos. En una reacción química, estas moléculas se descomponen y se combinan de diferentes maneras para formar nuevas sustancias.
Por ejemplo, si mezclas bicarbonato de sodio con vinagre, se produce una reacción química que genera dióxido de carbono, agua y acetato de sodio. En esta reacción, los átomos y las moléculas se reorganizan para formar estas nuevas sustancias, pero la cantidad total de materia sigue siendo la misma.
Otra manera de entender la ley de conservación de la materia es a través de las ecuaciones químicas. Estas ecuaciones muestran la reacción química de manera simplificada y nos permiten predecir qué sustancias se formarán y en qué cantidad.
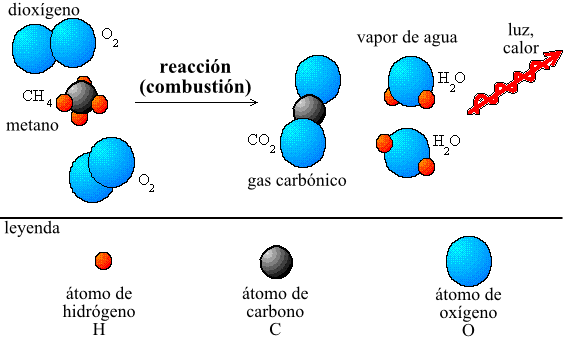
Por ejemplo, la ecuación química para la combustión del metano es:
CH4 + 2O2 → CO2 + 2H2O
Esta ecuación nos indica que un mol de metano (CH4) se combina con dos moles de oxígeno (O2) para formar un mol de dióxido de carbono (CO2) y dos moles de agua (H2O). Además, como la ley de conservación de la materia indica, la cantidad total de materia antes y después de la reacción es la misma.
La ley de conservación de la materia es una de las leyes fundamentales de la química que establece que la cantidad total de materia antes y después de una reacción química es la misma. Esta ley nos permite predecir qué sucederá en una reacción química y cómo se comportarán las sustancias involucradas. Además, nos ayuda a entender cómo se transforma la materia y cómo podemos controlar esas transformaciones.
- ¿Por qué es importante la ley de conservación de la materia?
- ¿Cómo se aplica la ley de conservación de la materia en la vida cotidiana?
- ¿Cuál es la relación entre la ley de conservación de la materia y la energía?
- ¿Por qué es importante equilibrar las ecuaciones químicas?
- ¿Qué sucede si la ley de conservación de la materia no se cumple en una reacción química?
¿Por qué es importante la ley de conservación de la materia?
La ley de conservación de la materia es importante porque nos permite entender cómo se comportan las sustancias en una reacción química. Además, nos permite predecir qué sustancias se formarán y en qué cantidad. Esta información es esencial para el diseño y la producción de productos químicos, medicamentos y materiales, entre otros.
¿Cómo se aplica la ley de conservación de la materia en la vida cotidiana?
La ley de conservación de la materia se aplica en la vida cotidiana de muchas maneras. Por ejemplo, al cocinar, al quemar combustible en un automóvil o al respirar. En todas estas situaciones, se producen reacciones químicas donde la cantidad total de materia antes y después de la reacción es la misma.
¿Cuál es la relación entre la ley de conservación de la materia y la energía?
La ley de conservación de la materia y la ley de conservación de la energía están relacionadas ya que ambas leyes establecen que la cantidad total de materia o energía no puede ser creada ni destruida, solo transformada. En una reacción química, la energía también se transforma junto con la materia.
¿Por qué es importante equilibrar las ecuaciones químicas?
Es importante equilibrar las ecuaciones químicas para asegurar que la cantidad total de materia antes y después de la reacción sea la misma. Al equilibrar la ecuación, se ajustan los coeficientes para que la cantidad de átomos de cada elemento sea la misma en ambos lados de la ecuación.
¿Qué sucede si la ley de conservación de la materia no se cumple en una reacción química?
Si la ley de conservación de la materia no se cumple en una reacción química, significa que la cantidad total de materia antes y después de la reacción no es la misma. Esto puede suceder si se pierde o se gana materia durante la reacción. En este caso, la ecuación química no estará equilibrada y no se podrá predecir con precisión qué sucederá en la reacción.
Deja una respuesta