Descubre la primera ley de la termodinámica: ¡energía que no se crea ni se destruye!
La termodinámica es una rama de la física que estudia la energía y sus transformaciones. La primera ley de la termodinámica es una de las más importantes y fundamentales en este campo, ya que establece que la energía no se puede crear ni destruir, sino que solo se puede transformar de una forma a otra.
Para entender mejor esta ley, imagina una pelota que se mueve de un lado a otro en una mesa. Cuando la pelota se mueve, tiene energía cinética, que se transforma en energía potencial cuando alcanza el punto más alto de su trayectoria. Si la pelota se detiene, su energía se transforma en calor debido a la fricción con la mesa. En ningún momento se ha creado o destruido energía, solo se ha transformado de una forma a otra.
La primera ley de la termodinámica se puede expresar matemáticamente como:
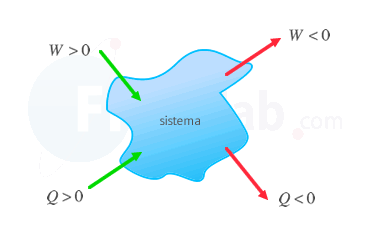
ΔU = Q - W
donde ΔU representa la variación de energía interna de un sistema, Q es el calor que se le suministra al sistema y W es el trabajo que realiza el sistema.
Esta ley se aplica a todos los sistemas, desde un pequeño objeto en movimiento hasta el universo en su conjunto. Nunca se crea ni se destruye energía, solo se transforma. Por ejemplo, la energía solar se transforma en energía química en las plantas durante la fotosíntesis, y luego se transforma en energía térmica cuando quemamos madera en una chimenea.
La primera ley de la termodinámica tiene importantes aplicaciones en la ingeniería y la tecnología. Por ejemplo, los motores de combustión interna transforman la energía química del combustible en energía mecánica, mientras que los paneles solares transforman la energía solar en energía eléctrica.
La primera ley de la termodinámica establece que la energía no se puede crear ni destruir, solo se puede transformar de una forma a otra. Esta ley es fundamental en la física y tiene importantes aplicaciones en la ingeniería y la tecnología.
- ¿Cómo se relaciona la primera ley de la termodinámica con la conservación de la energía?
- ¿Qué es la energía interna de un sistema?
- ¿Por qué es importante la primera ley de la termodinámica en la ingeniería y la tecnología?
- ¿Cómo se aplica la primera ley de la termodinámica en la vida cotidiana?
- ¿Qué es la segunda ley de la termodinámica?
¿Cómo se relaciona la primera ley de la termodinámica con la conservación de la energía?
La primera ley de la termodinámica y la conservación de la energía están estrechamente relacionadas. Ambas leyes establecen que la energía no se puede crear ni destruir, solo se puede transformar de una forma a otra. La conservación de la energía es un principio fundamental en la física, y la primera ley de la termodinámica es una expresión matemática de este principio.
¿Qué es la energía interna de un sistema?
La energía interna de un sistema es la energía total de todas las partículas que lo componen. Esta energía incluye la energía cinética y potencial de las partículas, así como la energía asociada con las interacciones entre ellas. La energía interna de un sistema puede variar debido a la transferencia de calor o trabajo, como se expresa matemáticamente en la primera ley de la termodinámica.
¿Por qué es importante la primera ley de la termodinámica en la ingeniería y la tecnología?
La primera ley de la termodinámica es importante en la ingeniería y la tecnología porque establece los límites de la energía disponible para realizar trabajo. Esta ley es fundamental para el diseño y la optimización de sistemas energéticos, como motores de combustión interna, turbinas de vapor y paneles solares. La comprensión de esta ley también es esencial para la eficiencia energética y la conservación de recursos.
¿Cómo se aplica la primera ley de la termodinámica en la vida cotidiana?
La primera ley de la termodinámica se aplica en muchas situaciones de la vida cotidiana. Por ejemplo, el calentamiento de una taza de café en el microondas se debe a la transferencia de energía desde el horno al líquido, como se expresa en la primera ley de la termodinámica. También se aplica en la refrigeración de alimentos, la producción de electricidad y el funcionamiento de vehículos y maquinarias.
¿Qué es la segunda ley de la termodinámica?
La segunda ley de la termodinámica establece que la entropía de un sistema cerrado siempre aumenta con el tiempo. La entropía es una medida de la cantidad de energía que no se puede utilizar para realizar trabajo útil. Esta ley implica que los procesos espontáneos siempre tienden a aumentar la entropía del universo, lo que se conoce como el principio de la entropía creciente. La segunda ley de la termodinámica tiene importantes implicaciones en la eficiencia energética y la sostenibilidad.
Deja una respuesta